Хеликобактериоз
Хеликобактериоз возникает из-за бактерии Helicobacter pylori. Она повреждает слизистую оболочку желудка и двенадцатиперстной кишки, вызывает воспаление и приводит к развитию хронического гастрита и язвы.
СОДЕРЖАНИЕ
Возбудитель хеликобактериоза
Пути передачи хеликобактер пилори
Симптомы хеликобактериоза
Осложнения хеликобактериоза
Диагностика хеликобактериоза
Общие сведения
Хеликобактериоз — инфекционное заболевание, которое вызывает бактерия хеликобактер пилори (Helicobacter pylori). С этим микроорганизмом ассоциируют хронический гастрит, язвенную болезнь желудка и двенадцатиперстной кишки, рак желудка и MALT-лимфому (опухолевое заболевание лимфоидной ткани слизистой оболочки желудка).
В России бактерию Helicobacter pylori обнаруживают у 65–92% взрослых.
В большинстве случаев заражение хеликобактером происходит в раннем детстве, взрослые инфицируются реже.
Основной фактор, влияющий на распространённость инфекции во всём мире, — уровень гигиены и санитарии, а также плотность населения. В некоторых странах наблюдается закономерность: чем младше поколение, тем меньше людей, инфицированных H. pylori, что можно связать с постепенным развитием санитарных служб и улучшением систем здравоохранения.
Возбудитель хеликобактериоза
Хеликобактериоз вызывает хеликобактер пилори (Helicobacter pylori) — спиралевидная бактерия, которая колонизирует пилорический отдел желудка, то есть его нижнюю часть, и двенадцатиперстную кишку.
Helicobacter pylori — спиралевидная бактерия. Она обладает 4–6 жгутиками, с помощью которых может быстро двигаться даже в густой слизи
Различные виды (штаммы) этой бактерии обладают разной патогенностью. Кроме того, способность хеликобактера вызывать поражение желудочно-кишечного тракта может меняться в зависимости от индивидуальных особенностей организма, который колонизирует бактерия.
H.pylori не всегда вызывает хеликобактерзависимые заболевания.
Пути передачи хеликобактер пилори
Точный способ передачи возбудителя до конца не выяснен. Различные исследования показали, что инфекция может сохранять жизнеспособность в воде в течение нескольких дней. Также удавалось обнаружить бактерии в стуле, слюне, налёте на зубах инфицированных.
Наиболее вероятные пути передачи бактерии:
- фекально-оральный — при несоблюдении мер личной гигиены. Например, если не мыть руки после посещения уборной и перед едой;
- орально-оральный — через слюну. Например, через поцелуи или при использовании общих столовых приборов, посуды и зубной щётки.
Хеликобактериозом можно заразиться при поцелуе
Течение хеликобактериоза
Попав в организм человека через рот, бактерия хеликобактер пилори достигает желудка. Там она быстро внедряется в его слизистую оболочку (эпителий), колонизирует её и начинает синтезировать вещества (в частности, уреазу), которые повышают локальную концентрацию аммиака. Аммиак выступает «щитом» для колонии бактерий: он нейтрализует соляную кислоту в желудочном соке и создаёт комфортную для хеликобактера щелочную среду.
Основное назначение слизистой оболочки желудка — защищать его стенки от воздействия соляной кислоты. Токсины, вырабатываемые хеликобактером, уничтожают клетки эпителия и разрушают его. Желудочный сок начинает разъедать оголённые стенки желудка, что приводит к химическому ожогу, воспалению и в некоторых случаях к появлению язв.
Helicobacter pylori — один из важнейших факторов риска рака желудка.
Кроме того, бактерия стимулирует иммунитет: мобилизуются разные виды клеток (эозинофилы, нейтрофилы, тучные клетки и др.), отвечающие за иммунную реакцию на месте и вызывающие воспаление. Также начинают продуцироваться антитела, которые защищают от патогена весь организм.
Если иммунитету не удаётся полностью уничтожить H. pylori, воспалительный процесс становится постоянным. Это способствует повреждению слизистой оболочки и развитию гастрита и язвы.
Хронический гастрит, ассоциированный с H. pylori, составляет 85–90% от всех форм хронического гастрита.
Без лечения бактерия H. pylori обычно продолжает населять организм в течение всей жизни человека.
Хронический гастрит проявляет себя болью в верхней части живота, нарушениями пищеварения и чувством дискомфорта после еды
Симптомы хеликобактериоза
Часто инфекция никак себя не проявляет. В этом случае говорят о бессимптомном носительстве.
Симптомы хеликобактериоза появляются только в том случае, если на фоне инфекции развиваются воспалительные заболевания — хронический гастрит, язва желудка или двенадцатиперстной кишки и другие. В этих случаях клиническая картина будет соответствовать заболеванию.
Общие симптомы эрозивно-язвенного поражения желудка и двенадцатиперстной кишки:
- боль в животе;
- нарушения пищеварения — снижение аппетита, изжога, отрыжка, тошнота, рвота, дискомфорт в животе после еды;
- общее недомогание;
- снижение веса.
Живот болит в эпигастральной области — по центру под грудной клеткой. Боль может появляться сразу после еды, через 30–40 минут, 1–1,5 часа или даже через 2 часа — период зависит от заболевания и особенностей его течения.
При язве двенадцатиперстной кишки наблюдаются «голодные боли» — возникают на пустой желудок и проходят после еды. Также для этого заболевания характерны астенический синдром (повышенная усталость, плохое настроение) и кровотечения (проявляются в виде чёрного стула либо рвоты с примесью крови).
Среди проявлений хеликобактериоза также есть внекишечные, то есть не связанные с заболеваниями желудочно-кишечного тракта.
Внекишечные проявления хеликобактериоза:
- железодефицитная анемия — состояние, при котором снижается уровень красных клеток крови из-за нехватки железа;
- хроническая иммунная тромбоцитопения — заболевание, при котором уменьшается количество тромбоцитов.
Осложнения хеликобактериоза
Патогенные штаммы H. pylori вызывают воспаление слизистой оболочки желудка или двенадцатиперстной кишки. В результате развивается хронический гастрит и дуоденит. У большинства людей он может никак не проявляться на протяжении всей жизни. Если хеликобактериоз не лечить, могут развиться более тяжёлые заболевания.
Распространённые осложнения хеликобактериоза:
- язвенная болезнь;
- рак желудка;
- MALT-лимфома (опухолевое заболевание лимфоидной ткани слизистой оболочки желудка).
Кроме того, инфекция H. pylori увеличивает риск кровотечений и образования язв у пациентов, принимающих нестероидные противовоспалительные препараты (например, аспирин).
Диагностика хеликобактериоза
Золотым стандартом в диагностике хеликобактериоза считается гистологическое исследование. У пациента во время фиброгастродуоденоскопии (ФГДС) берут биоматериал из желудка. В лаборатории его окрашивают с помощью специальных составов и затем изучают под микроскопом.
ФГДС — визуальный осмотр слизистой оболочки пищевода, желудка и двенадцатиперстной кишки при помощи эндоскопа, вводимого в желудок через рот
Этот метод позволяет не только обнаружить хеликобактер пилори в исследуемом образце, но также оценить характер повреждений слизистой оболочки.
15.34. 
3 дня

Похожим образом проводится эндоскопическое исследование. Отличие состоит в том, что при таком анализе осматривают слизистую оболочку только желудка.
14.12. Соскоб (+450 ₽) 
Соскоб (+450 ₽) 3 дня

Один из наиболее точных и информативных способов установить факт инфицирования — исследование кала на присутствие в нём антигенов (частиц бактерии) H. pylori методом иммуноферментного анализа.
Можно исследовать биоматериал на наличие в нём генетического материала (ДНК) хеликобактер пилори. Наиболее эффективным в этом случае будет метод полимеразной цепной реакции (ПЦР), который позволяет обнаружить даже очень малое количество микроорганизмов. ДНК, как правило, ищут в кале, так как бактерия обычно обитает в желудке или кишечнике.
19.37.1. 
Кач. 2 дня

19.72.2. 
2 дня

Также для анализа могут взять соскоб из полости рта — такой способ часто применяется при обследовании детей из-за его безболезненности.
19.72.1. Соскоб (+450 ₽) 
Соскоб (+450 ₽) 2 дня

19.37.2. Соскоб (+450 ₽) 
Соскоб (+450 ₽) 2 дня

Хеликобактерная инфекция вызывает иммунный ответ, который сопровождается синтезом антител IgA, IgM, IgG.
20.86. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) 2 дня

20.87. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) Колич. 2 дня

20.14. Вен. кровь (+220 ₽) 
Вен. кровь (+220 ₽) Колич. 3 дня

Ещё один способ выявить инфекцию — бактериологическое исследование, или посев. Микроорганизмы засевают в питательную среду и наблюдают за их ростом. Анализ трудоёмкий и дорогостоящий, однако обладает стопроцентной точностью. Кроме того, с его помощью можно определить штамм бактерии, антибиотик, к которому она наиболее восприимчива, а также оценить эффективность терапии (посев проводится через 4 недели после завершения лечения).
Безболезненный способ обнаружить H. pylori — дыхательный уреазный тест. Он основан на способности бактерии выделять уреазу. Пациенту дают выпить специально подготовленный раствор мочевины, в котором содержатся помеченные атомы углерода. Уреаза расщепляет мочевину на аммиак и углекислый газ, который с кровью переносится в лёгкие. Через 15–30 минут пациента просят подышать в трубочку, чтобы проанализировать состав выдыхаемого воздуха. Тест-система фиксирует концентрацию меченого углерода, благодаря чему определяют, есть ли инфекция.
Ещё один аналогичный метод обнаружения хеликобактера — «Хелик-тест». Отличие заключается только в специальном растворе, который пациент выпивает во время исследования: здесь используется карбамид. В остальном процедура и суть исследования такие же.
К какому врачу обращаться при хеликобактериозе
Заподозрить Helicobacter pylori и назначить анализы может гастроэнтеролог — врач, который занимается диагностированием, лечением и профилактикой заболеваний желудочно-кишечного тракта.
Обычно на приём к гастроэнтерологу пациент попадает по направлению от терапевта или другого специалиста.
Лечение хеликобактериоза
Лечить хеликобактерную инфекцию рекомендуется только в том случае, если у пациента есть воспалительные заболевания желудка или двенадцатиперстной кишки. Начинать антибактериальную терапию исключительно из-за обнаружения H. pylori необязательно.
Если у пациента есть показания для эрадикации (уничтожения) H. pylori, ему назначают лечение антибиотиками. Существует несколько терапевтических схем, включающих один, два или три антибактериальных препарата. Также терапию могут дополнять средствами, угнетающими секрецию кислоты, и препаратами висмута.
Лечение занимает 2 недели.
Эффективность лечения оценивают через 2–6 недель после последнего приёма лекарства.
Прогноз и профилактика
Как правило, при соблюдении рекомендаций врача прогноз благоприятный: хеликобактер пилори уничтожается полностью.
Однако важно учитывать, что возможно заразиться повторно. Избежать этого можно с помощью несложной профилактики.
Основные меры профилактики хеликобактериоза:
- соблюдение правил личной гигиены;
- укрепление иммунитета;
- своевременное лечение заболеваний желудочно-кишечного тракта;
- обследование людей, контактировавших с инфицированными хеликобактером;
- плановые профилактические обследования.
Правила личной гигиены, которые рекомендуется соблюдать:
- мыть руки после посещения туалета и перед едой;
- использовать только личные предметы и средства гигиены (полотенца, зубные щётки и др.);
- не есть из одной тарелки с другими людьми и пользоваться индивидуальными столовыми приборами.
Чтобы избежать заражения хеликобактером, рекомендуется использовать только личные предметы гигиены
Источники
- Ивашкин В. Т., Маев И. В., Лапина Т. Л. и др. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых // Российский журнал гастроэнтерологии, гепатологии, колопроктологии, 2018. № 28(1). С. 55–70.
- Минушкин О. Н., Зверков И. В., Львова Н. В., Скибина Ю. С., Иневатова В. С. Хронический гастрит: современное состояние проблемы // Терапевтический архив, 2020. Т. 92. № 8. C. 18–23.
- Parikh N. S., Ahlawat R. Helicobacter Pylori // StatPearls.
- Katelaris P., Hunt R., Bazzoli F. Глобальные практические рекомендации Всемирной гастроэнтерологической организации. 2021.
Частые вопросы
Считается, что хеликобактер пилори передаётся от человека человеку при нарушении правил личной гигиены, а также через слюну.
Точный способ передачи хеликобактериоза не выяснен. Наиболее вероятными считаются фекально-оральный и орально-оральный (через слюну) пути передачи.
Обычно при хеликобактериозе болит живот в области под грудной клеткой, снижается аппетит, появляется изжога, отрыжка, тошнота, рвота, дискомфорт в животе после еды.
Хеликобактер пилори разрушает слизистую оболочку желудка и двенадцатиперстной кишки, повреждает стенки этих органов, вызывая воспаление — гастрит.
Если у пациента есть показания для уничтожения H. pylori, ему назначают лечение антибиотиками. Также могут назначить препараты, снижающие выработку кислоты и защищающие слизистую оболочку желудка.
Информацию проверил
врач-эксперт
Информацию проверил врач-эксперт
Екатерина Кашух
Врач-гастроэнтеролог, кандидат медицинских наук
Оцените статью:
Полезная статья? Поделитесь в социальных сетях:
ВАЖНО
Информация из данного раздела не может служить достаточным основанием для постановки диагноза или назначения лечения. Решение об этом должен принимать врач на основании всех имеющихся у него данных.
Вам может быть интересно
Вам телеграм.
Telegram-канал,
которому, на наш взгляд,
можно доверять
- ИНВИТРО
- Библиотека
- Справочник заболеваний
- Хеликобактериоз…
Хеликобактериоз (хеликобактер пилори, хеликобактерная инфекция, Helicobacter pylori, H. pylori)
Хеликобактериоз: причины появления, симптомы, диагностика и способы лечения.
Определение
Хеликобактериоз – это инфекционное заболевание, поражающее пилорический отдел желудка, или привратник, и двенадцатиперстную кишку. Его возбудителем является уникальная патогенная микроаэрофильная грамотрицательная бактерия хеликобактер пилори (H. pylori). Свое название бактерия получила за счет отдела желудка, в котором она обитает – пилорического.
В результате своей жизнедеятельности H. pylori формирует вокруг себя «облако» щелочной среды, что позволяет этой бактерии выживать в агрессивной кислотной среде желудка, вызывая ускоренную секрецию соляной кислоты, а также снижение секреции щелочи в двенадцатиперстной кишке.
В результате микроорганизм еще сильнее колонизирует слизистую оболочку, формирует ее повышенную восприимчивость к соляной кислоте и провоцирует воспаление, приводящее к развитию язвенных дефектов.
Хеликобактер пилори – спиралевидная бактерия длиной 3,5 и шириной 0,5 микрон. Она имеет жгутики, с помощью которых свободно перемещается по стенке желудка либо надежно на ней закрепляется. Бактерия H. pylori очень изменчива, ее штаммы (разновидности) отличаются друг от друга способностью прикрепляться к слизистой оболочке желудка, вызывать воспалительный процесс и обладают разной степенью патогенности.
Хеликобактер пилори, колонизирующая слизистую оболочку желудка, — частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием. В зависимости от состояния защитных факторов желудка возникший инфекционный процесс может протекать латентно или с выраженной клинической симптоматикой воспаления. Согласно современным представлениям, H. pylori вызывает хронический гастрит у всех зараженных лиц. Это может привести к язвенной болезни, атрофическому гастриту, аденокарциноме желудка или низкодифференцируемой лимфоме желудка. H. pylori относится к канцерогенам первого порядка.
Результаты многочисленных исследований дают основание предполагать возможную патогенетическую или опосредованную роль инфекции H. pylori в развитии и/или течении заболеваний, не относящихся к пищеварению: кардио-, цереброваскулярных, аутоиммунных заболеваний, заболеваний крови, кожи, нервной системы и многих других.
Патоген отличается относительной устойчивостью к окружающей среде: при кипячении хеликобактерии гибнут практически мгновенно, при обработке дезинфицирующими составами — в течение нескольких минут.
Причины появления хеликобактериоза
Заразиться бактерией можно при контакте с загрязненной водой или продуктами питания. Инфицирование возможно во время проведения эндоскопии и при использовании других плохо стерилизованных медицинских инструментов, которые имели прямой контакт со слизистой желудка пациента.
Бытовой способ передачи (например, через поцелуи, личные вещи и проч.) также возможен, о чем свидетельствует выделение бактерии из слюны и зубного налета.
Распространенность инфекции варьируется в зависимости от географического региона, возраста пациента, его этнической принадлежности и социально-экономического статуса. По данным Департамента здравоохранения г. Москвы (2019), распространенность этой инфекции в Москве составляет 60,7–88%, в Санкт-Петербурге — 63,6%, в Восточной Сибири достигает 90%.
Классификация заболеваний
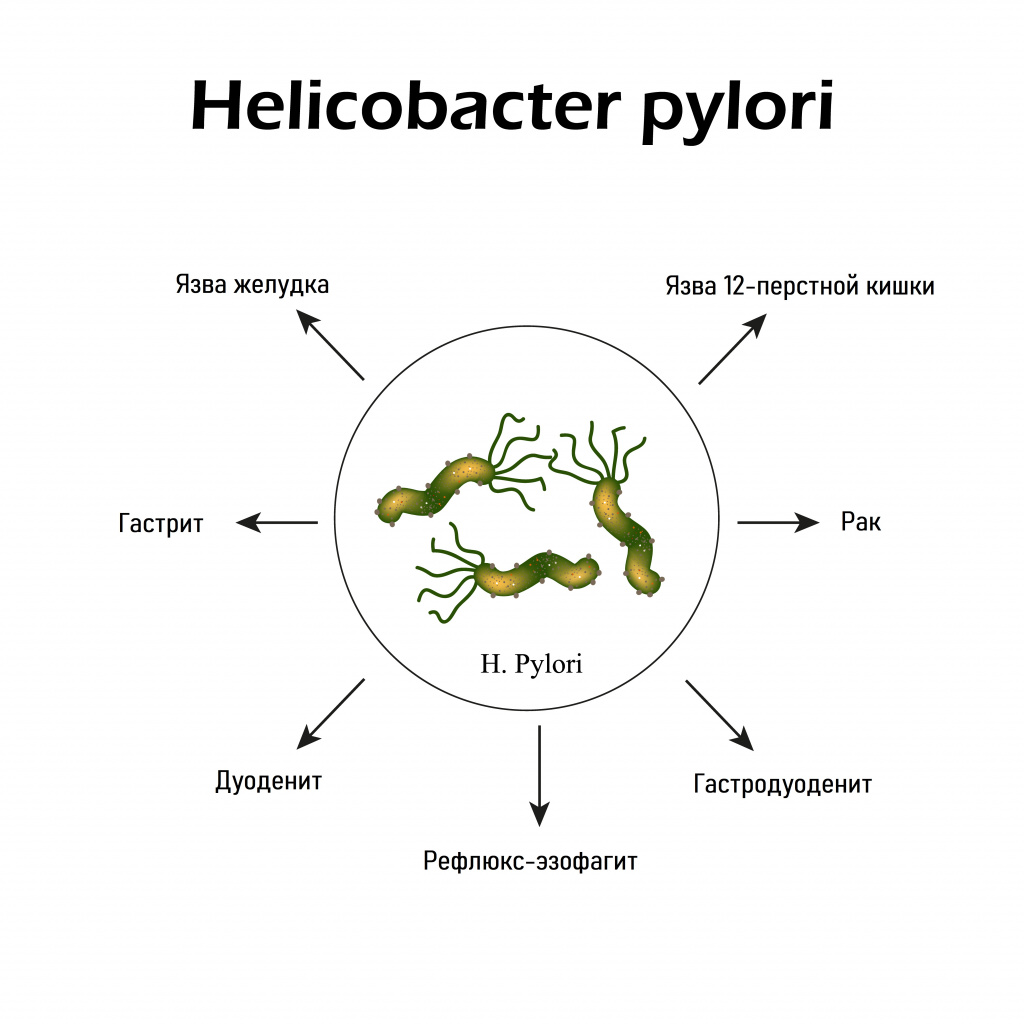
Заболевания, связанные с H. pylori:
- гастрит,
- дуоденит,
- гастродуоденит,
- эзофагит,
- язвенная болезнь желудка,
- язвенная болезнь двенадцатиперстной кишки,
- железодефицитная анемия неясного генеза,
- рак желудка,
- рак двенадцатиперстной кишки.
Основным проявлением Helicobacter pylori является хроническое воспаление желудка. В случае быстрой первичной манифестации возбудителя острый период хеликобактериоза длится около 10 дней. Общее состояние больных обычно остается удовлетворительным, иногда отмечается кратковременная субфебрильная температура, снижение работоспособности.
Основной жалобой, с которой больные с признаками Helicobacter-инфекции обращаются к врачу, являются желудочные боли. Локализация симптома может меняться и переходить в область расположения двенадцатиперстной кишки.
Боли бывают острыми, ноющими, тупыми, возникают в верхних отделах живота слева и по центру в околопупочной области. Дискомфорт может возникать при длительном голодании, натощак или через определенное время после приема пищи.
Симптоматика хеликобактериоза зависит от клинической формы заболевания и может включать:
- чувство тяжести в животе после еды;
- нарушение аппетита, связанное с внезапными приступами тошноты (если слизистая желудка сильно травмирована);
- беспричинная рвота на фоне нормальной температуры тела;
- изжога (жгучие ощущения в пищеводе и даже гортани) и отрыжка с неприятным кислым или горьким привкусом;
- хронические запоры (отсутствие дефекации в течение трех суток и более);
- разжижение каловых масс, появление пенистой или водянистой консистенции;
- кишечные спазмы и вздутие живота.
При сильном обсеменении хеликобактериями может возникнуть и ряд нетипичных симптомов, которые свидетельствуют о значительном заражении и прогрессировании болезни:
- снижение аппетита до полного его отсутствия;
- тошнота может сменяться рвотой со сгустками крови;
- резкое снижение массы тела, не являющееся нормой;
- сухость во рту и привкус металла;
- появление белого налета на языке;
- неприятный запах изо рта при отсутствии кариеса;
- заеды в уголках рта;
- кровоточивость десен.
При хроническом течении заболевания и атрофическом поражении слизистой желудка возникают признаки железодефицитной анемии — частые головные боли и головокружения, бледность кожных покровов, снижение артериального давления и тахикардия.
Диагностика хеликобактериоза
Долгое время хеликобактериоз может никак себя не проявлять, при этом провоцируя развитие язвы, аденокарциномы или мальтомы желудка. В особой зоне риска люди, чьи родственники имеют эти заболевания в анамнезе.
Диагностика может быть инвазивной (эндоскопия с последующей биопсией желудочных тканей) и неинвазивной (лабораторные исследования).
Согласно международным рекомендациям, методами выбора для диагностики бактерии и оценки эффективности лечения H. pylori служат дыхательный̆ тест с мочевиной, меченной 13С и определение специфических антигенов H. pylori в кале иммунохроматографическим методом.
Для ранней диагностики H. pylori-ассоциированного хронического гастрита, оценки характера и тяжести патологического процесса разработана комплексная лабораторная «Гастропанель», в дополнение к которой оценивают гастрин — полипептидный гормон ЖКТ, регулирующий секрецию соляной кислоты, моторику и пролиферацию клеток слизистой желудка.
Гастрин-17 (стимулированный)
Синонимы: Анализ крови на гастрин; Малый гастрин; Гастрин с нагрузкой; Гастрин-17 после белковой стимуляции.
Gastrin-17; G-17; G-17s; Gastrin-17 Stimulation Test.
Краткая характе�…
Для обнаружения первичной инфекции используется определение иммуноглобулинов класса G в крови.
Антитела к Helicobacter pyl. IgG (блот)
Высокоспецифичный тест, выявляющий факт инфицирования H. pylori.
Метод Вестерн-блота для определения антител к H. Pylori, в отличие от обычного ИФА, даёт дифференциров�…
В качестве метода первичной диагностики у лиц, имеющих показания к проведению эндоскопического исследования желудка и 12-перстной кишки (гастроскопии), производится забор биоптата из антрального отдела и тела желудка, которые изучают морфологически и на наличие хеликобактерий:
Гастроскопия
Исследование слизистой оболочки верхнего отдела желудочно-кишечного тракта с возможностью выполнения биопсии или эндоскопического удаления небольших патологич…
- выявление ДНК H. pylori в биоптате используется для подтверждения инфицированности и обоснования антибактериальной терапии при гастродуодените, язвенной болезни желудка и двенадцатиперстной кишки;
Тесты показаны следующим категориям пациентов:
- пациентам, имеющим характерную симптоматику;
- пациентам с выявленной язвенной болезнью желудка или двенадцатиперстной кишки;
- пациентам с семейной историей рака желудка;
- пациентам с атрофическим гастритом;
- пациентам с дефицитом железа неясного генеза.
В первую очередь, проводят дифференциальную диагностику хеликобактериоза, чтобы отличить его от функциональной диспепсии. Основными диагностическими критериями, свидетельствующими в пользу хеликобактериоза, являются наличие воспалительных изменений слизистой желудка и двенадцатиперстной кишки, выявление H. рylori с помощью эндоскопии. В остром периоде болезнь нужно дифференцировать с кишечными инфекциями.
К каким врачам обращаться
Кроме врача-гастроэнтеролога для обследования пациента привлекают врачей-терапевтов или врачей общей практики (семейных врачей), инфекционистов, хирургов, эндоскопистов.
Лечение хеликобактериоза
Выбор тактики лечения зависит от клинического течения патологии.
Хронический гастрит, вызванный инфекцией Н. pylori, в том числе у больных с бессимптомным течением, можно рассматривать как показание к проведению терапии хеликобактериоза.
Терапия направлена:
- на быстрое заживление язв желудка и двенадцатиперстной кишки;
- снижение риска рецидивов язвенной болезни;
- снижение риска язвенных кровотечений;
- снижение риска развития рака желудка;
- разрешение железодефицита и/или повышение эффективности его лечения.
Основные группы препаратов:
Антибактериальные средства. Микроорганизм быстро вырабатывает сопротивляемость к антибактериальным веществам, что значительно затрудняет процесс лечения. Иногда врачу приходится комбинировать сразу несколько препаратов, чтобы добиться положительной динамики.
Ингибиторы протонной помпы — антисекреторные препараты, снижающие кислотность желудочного сока и повышающие эффективность антибиотиков.
Коллоидные соли висмута. Препараты, содержащие висмут, оказывают бактерицидное действие, усиливают защитные факторы слизистой желудка.
Пробиотики. Дополнительное включение в схему лечения пробиотиков позволяет повысить эффективность терапии и снизить риск возникновения нежелательных побочных явлений.
Продолжительность любой схемы лечения H. pylori должна составлять не менее 14 дней. Контрольные исследования следует проводить не раньше, чем через месяц после окончания лечения на фоне отмены приема ингибиторов протонной помпы (они входят во все схемы терапии). Контрольную гастроскопию выполняют не ранее, чем через год.
Особую проблему составляет лечение H. Pylori в педиатрии. Течение болезни у детей и взрослых существенно различается, а терапия не всегда оправдана:
- у детей меньше клинических проявлений заболеваний, вызванных H. pylori;
- низкий риск появления осложнений одновременно с высоким риском повторного инфицирования;
- не все тесты и методы применимы в детской гастроэнтерологии;
- больше противопоказаний к антибактериальным препаратам, сложнее подобрать адекватные схемы дозирования и определить длительность приема;
- быстрое появление резистентности инфекционного агента к препаратам.
Осложнения
При своевременном начале лечения можно предотвратить опасные последствия заболевания и исключить риск заражения других людей.
Одно из частых последствий хеликобактериоза — усиление выработки соляной кислоты и гастрина, снижение факторов защиты, приводящее к возникновению хронического или атрофирующего гастрита. По мере прогрессирования заболевания формируются участки атрофии слизистой оболочки желудка, снижается кислотность.
При хеликобактериозе нарушается всасывание витамина В12. У пациентов развиваются признаки анемии и поражается периферическая нервная система.
Атрофия эпителиального слоя желудка может влиять на развитие патологических эндокринных процессов. Наиболее опасное осложнение — метаплазия и дисплазия атрофированной слизистой, значительно повышающая риск рака желудка.
Профилактика хеликобактериоза
Профилактика хеликобактериоза включает соблюдение правил личной гигиены, рациональное питание, лабораторное обследование людей, которые были в контакте с инфицированным H. рylori.
Чтобы избежать заражения, необходимо тщательно мыть руки; использовать только свои средства и предметы гигиены (полотенца, зубные щетки и т. д.); полностью излечивать заболевания желудочно-кишечного тракта; проходить плановые профилактические медицинские обследования.
Наиболее эффективной̆ мерой̆ профилактики осложнений заболевания является эрадикационная терапия инфекции Н. pylori при хроническом гастрите, в том числе при бессимптомном течении. Устранение H. pylori приводит к излечению гастрита, что является основой профилактики долгосрочных осложнений или рецидивов болезни.
Для закрепления результатов лечения и укрепления иммунитета назначают витаминные комплексы и ряд микроэлементов.
Источники:
- Ивашкин В.Т., Маев И.В., Лапина Т.Л. с соавт. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2018; 28(1):55-70.
- Бордин Д.С., Эмбутниекс Ю.В., Хомерики С.Г. Методы диагностики инфекции Helicobacter pylori. Методические рекомендации. Департамент здравоохранения города Москвы. 2019, 36 с.
- Жебрун А.Б., Лазебник Л.Б., Ткаченко С.Б. с соавт. Диагностика и лечение заболеваний желудочно-кишечного тракта, ассоциированных с инфекцией Helicobacter pylori. Практическое руководство для врачей. Москва. 2006.
- Клинические рекомендации «Гастрит и дуоденит». Разраб.: Российская Гастроэнтерологическая Ассоциация, Ассоциация «Эндоскопическое общество «РЭндО». – 2021.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.
Информация проверена экспертом

Лишова Екатерина Александровна
Высшее медицинское образование, опыт работы — 19 лет
Поделитесь этой статьей сейчас
Рекомендации
-
13062
01 Марта
-
13062
23 Февраля
-
4422
21 Февраля
Похожие статьи
Псевдотуберкулез
Псевдотуберкулез: причины появления, симптомы, диагностика и способы лечения.
Описторхоз
Описторхоз: причины появления, симптомы, диагностика и способы лечения.
Сифилис
Сифилис: причины появления, симптомы, диагностика и способы лечения.
Амилоидоз
Амилоидоз: причины появления, симптомы, диагностика и способы лечения.
Ботулизм
Ботулизм: причины появления, симптомы, диагностика и способы лечения.
Еще не так давно считалось, что гастрит вызывают неправильное питание, еда всухомятку, стрессы и отсутствие горячего супа на обед. Потом ученые обнаружили связь этой болезни с бактерией хеликобактер пилори — и с тех пор подход к лечению заболеваний ЖКТ кардинально изменился.
Можно ли заразиться через посуду в ресторане, вызывает ли хеликобактер рак и нужно ли избавляться от бактерии, которая живет в организме 80% белорусов, рассказал врач-гастроэнтеролог с 40-летним опытом работы Георгий Матвеевич Усов.
Георгий Усов,
врач-гастроэнтеролог высшей категории
Минского клинического консультативно-диагностического центра,
кандидат медицинских наук
— Что такое хеликобактер? Это патогенная бактерия или условно-патогенная?
— Хеликобактер пилори (Helicobacter pylori) — бактерия, которая была открыта австралийскими учеными Робином Уорреном и Барри Маршаллом. За это открытие в 2005 году они получили Нобелевскую премию.
Хеликобактер — патогенная бактерия. Наличие ее в организме человека приводит к поражению слизистой оболочки желудка и двенадцатиперстной кишки и развитию таких заболеваний, как хронический гастрит, язва желудка и двенадцатиперстной кишки, рак желудка, мальтома желудка.
Сегодня хеликобактер — самая распространенная хроническая инфекция в мире.
— Какие факторы в таком случае провоцируют развитие гастрита, язвы, рака? И могут ли эти болезни возникнуть без участия хеликобактера?
— При наличии хеликобактера у всех людей выявляется какое-либо заболевание желудка. Выявление конкретного заболевания зависит от штамма хеликобактера. Штаммы H. руlori, имеющие в своем составе определенные генотипы, предрасполагают к развитию язвенной болезни и рака желудка. И если язвой желудка и двенадцатиперстной кишки или онкологическими заболеваниями заболевают не все инфицированные люди, то гастритом — все.
Верно и то, что данные болезни могут возникать и без хеликобактер пилори.
- Кроме гастритов, связанных с хеликобактером, имеются гастриты, связанные с забросом содержимого двенадцатиперстной кишки в желудок, так называемые рефлюксные (химические) гастриты, гастриты, связанные с образованием антител к слизистой оболочке желудка (аутоиммунные гастриты).
- Причиной язв может быть прием нестероидных противовоспалительных препаратов, ацетилсалициловой кислоты, изредка нервные факторы, погрешности в еде.
- Причиной раковых заболеваний могут быть погрешности в питании, канцерогенные вещества, поступающие в пищу, курение, наследственная предрасположенность и др.
— Как передается эта бактерия человеку? Можно ли заразиться от животных? А в ресторане через посуду?
— Путь передачи хеликобактера контактно-бытовой. Бактерия передается:
- через недостаточно чистую посуду, когда люди едят из одной тарелки или пьют из одной чашки, едят пищу друг у друга;
- в семье, когда родители пробуют пищу перед тем, как дать ее ребенку, или облизывают соску малыша;
- в случае использования людьми одной зубной щетки;
- через губную помаду;
- при отсутствии мытья рук после туалета и перед едой;
- через сексуальные поцелуи.
Хеликобактер также выявлен у кошек и собак, вследствие чего существует возможность заражения человека от них. Что касается ресторана, то, если грязная посуда плохо обрабатывается, появляется высокая возможность заражения хеликобактером.
— Какой процент людей в Беларуси живет с хеликобактером? Почему этот показатель выше, чем в Западной Европе и США?
— Качественных эпидемиологических исследований по распространению хеликобактера среди населения Беларуси не проводилось. Проводились лишь относительно небольшие исследования среди населения отдельных областей и отдельных групп населения.
Считается, что распространенность хеликобактера среди белорусов составляет около 70-80%.
Среди населения РФ по ряду исследований в отдельных российских регионах распространенность составляет от 65 до 90%. Данный показатель выше, чем в Западной Европе и США, в связи с недостаточно качественным соблюдением гигиены в нашей стране.
— Какие симптомы должны заставить человека сдать анализ на хеликобактер? Какие из них неочевидные, не связанные напрямую с ЖКТ?
— Диспепсические расстройства (боли, жжение в эпигастральной области — верхних отделах живота, тошнота, плохой аппетит, тяжесть в эпигастральной области, рвота и т. д.) требуют обследования на хеликобактер.
В некоторых случаях хеликобактер может быть причиной также:
- железодефицитной анемии;
- халитоза (плохого запаха изо рта);
- крапивницы.
Однако следует помнить, что данные заболевания могут возникать и по множеству других причин.
— Какие анализы на выявление хеликобактер существуют? Какие из них самые объективные?
— Существует несколько разновидностей анализов.
- Гистологическое исследование биопсийного материала из слизистой желудка, причем следует исследовать слизистую как антрального отдела, так и тела желудка.
- Быстрый уреазный тест. Тест выполняется в момент гастроскопии. Биопсия слизистой берется из полости желудка, помещается в среду, содержащую мочевину и такой индикатор, как феноловый красный. Уреазы преобразуют мочевину в аммиак, вследствие чего повышается рН среды, и желтый цвет образца (отрицательный) меняется на красный (положительный).
- С13-уреазный дыхательный тест на немецкой аппаратуре, достоверность которого более 92%.
- Российская модификация дыхательного теста — хелик-тест, достоверность которого, по данным ряда российских авторов, составляет от 30 до 80%.
- Определение антител к хеликобактеру IgM и IgG в крови.
- Исследование антигенов хеликобактера в кале.
Самыми объективными из анализов являются гистологический тест, С13-уреазный дыхательный тест на аппаратуре немецкой фирмы FAN, исследование антигенов хеликобактера в кале и быстрый уреазный тест. Исследование крови на антитела к хеликобактер пилори приемлемо при первичном исследовании до лечения хеликобактера. В то же время для контрольного исследования оно не годится, так как антитела к хеликобактеру остаются повышенными в течение нескольких лет в крови после излечения от хеликобактера, давая ложноположительный результат.
Хелик-тест из-за низкой достоверности нигде в мире, кроме нескольких стран СНГ, не применяется.

— Что делать, если анализ положительный? Влияет ли, например, количественное значение антител в крови на степень опасности бактерии для здоровья?
— При положительном анализе на хеликобактер решается вопрос о проведении антихеликобактерной терапии. На степень опасности для здоровья количественное значение хеликобактера существенного значения не имеет, ибо высокая обсемененность хеликобактером в ряде случаев в наших исследованиях приводила к значительно меньшим изменениям слизистой оболочки, чем низкая, или существенно не отличалась. Причина — в индивидуальной резистентности (восприимчивости) организма к хеликобактеру.
При незначительных превышениях IgA желательно провести другой метод исследования хеликобактера, например С13-уреазный дыхательный тест или исследование кала на антигены хеликобактера, чтобы подтвердить или опровергнуть положительный результат.
— Всегда ли положительный анализ говорит о необходимости лечения? В каких случаях хеликобактер не лечат?
— Раньше считалось, что лечение хеликобактера следует проводить, только если имеются клинические проявления заболевания. Сейчас в связи с выявлением существенной роли хеликобактера в развитии рака желудка лечение рекомендуют проводить всем больным с хеликобактерной инфекцией.
В некоторых странах, в частности, Японии, лечение хеликобактера проводится всем больным бесплатно. При этом тем людям, которые отказываются лечиться от хеликобактера, при развитии у них рака желудка не оплачивают страховку.
У лиц с язвами желудка и двенадцатиперстной кишки санация хеликобактера приводит к уменьшению появления новых язв в три раза.
Лечение хеликобактера НЕ проводят:
- больным с аллергией и/или непереносимостью препаратов, предназначенных для лечения хеликобактера;
- тем, у кого все схемы лечения оказались неэффективными;
- отказывающимся от лечения пациентам.
На мой взгляд, больным с хроническим гастритом, у которых имеются лишь незначительные изменения слизистой оболочки желудка, от лечения можно временно воздержаться.
Лечение детей не проводят: существует большая вероятность повторного заражения из-за нахождения в детском коллективе и развития ряда побочных реакций, особенно при повторном лечении. Для детей желательно выделение отдельной посуды и соблюдение правил личной гигиены.
— Какое лечение назначается?
— Излечиться от хеликобактера полностью возможно только при назначении антибиотиков и блокаторов протоновой помпы (антисекреторных лекарственных средств — прим. ред.), усиливающих эффект антибиотиков, в ряде случаев в сочетании с препаратами висмута.
В последнее время выявлено бактерицидное действие некоторых пробиотиков в отношении хеликобактера.
Например, существует препарат, содержащий инактивированные бактерии пробиотического штамма Lactobacillus reuteri. Однако подобные препараты полностью от хеликобактера не излечивают.
— Должны ли параллельно лечиться домашние? Может ли такое быть, что у одного из членов семьи есть хеликобактер, а у остальных — нет?
— Да, лечение взрослых членов семьи при наличии у них хеликобактера должно проводиться, детям из-за указанных выше причин — нет. При этом наличие хеликобактера у всех членов одной семьи необязательно. Это зависит от индивидуальной резистентности организма к бактерии. В исследованиях и клинической практике неоднократно были случаи, когда хеликобактер не обнаруживался у отдельных членов семьи. Поэтому лечению всегда должны предшествовать анализы.

Версия: Клинические рекомендации РФ 2018-2020 (Россия)
Категории МКБ:
Гастродуоденит неуточненный (K29.9), Диспепсия (K30), Язва двенадцатиперстной кишки (K26), Язва желудка (K25)
Разделы медицины:
Гастроэнтерология
Общая информация
Краткое описание
Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых
Введение
Необходимость обновления «Рекомендаций Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых» [1] обусловлена тем, что в последние годы были выполнены новые отечественные и зарубежные клинические исследования по ведению больных с H. pylori-ассоциированными заболеваниями, а также разработаны ключевые международные документы, такие как Киотский консенсус [2] и консенсус Маастрихт V Европейской группы по изучению Helicobacter и микробиоты [European Helicobacter and Microbiota Study Group (EHMSG)] [3].
19 мая 2017 г. под председательством президента Российской гастроэнтерологической ассоциации (РГА) академика РАН В.Т. Ивашкина состоялось заседание Экспертного совета РГА, на котором были рассмотрены вопросы оптимизации эрадикационной терапии инфекции H. pylori в рамках подготовки настоящей редакции Рекомендаций [4], ее положения были представлены для дискуссии в рамках 23-й Объединенной Российской гастроэнтерологической недели (9–11 октября 2017, г. Москва).
Согласно данным из различных регионов нашей страны, инфекцию H. pylori обнаруживают у 65–92% взрослых [4], в связи с чем вопросы ее диагностики и лечения крайне актуальны для практики врачей различных специальностей. Высокая частота формирования хронического геликобактерного гастрита обусловливает высокую частоту развития других заболеваний, ассоциированных с H. pylori. В нашей стране ежегодно регистрируют более 37 тыс. новых случаев рака желудка, который занимает 4-e место в структуре онкологической заболеваемости и 2-е место в структуре смертности при онкологических заболеваниях.
Цель рекомендаций — ознакомить практикующих врачей с показаниями к проведению антигеликобактерной терапии, методами и порядком проведения диагностики и эрадикационной терапии инфекции H. pylori.
Показания к проведению эрадикационной терапии инфекции H. pylori
Современная классификация хронического гастрита основана на этиологическом подходе. Бактерия H. pylori, колонизирующая слизистую оболочку желудка, — наиболее частая причина ее воспалительных изменений, она признана этиологическим фактором гастрита, а сам гастрит — инфекционным заболеванием [2]. Хронический геликобактерный гастрит служит фоном для развития болезней, ассоциированных с Н. pylori, в том числе рака желудка [3, 5]. С точки зрения современной гастроэнтерологии, наиболее эффективной мерой профилактики рака желудка является эрадикационная терапия инфекции Н. pylori при хроническом гастрите, в том числе у «бессимптомных» лиц [6, 7]. Степень снижения риска развития рака желудка после успешной антигеликобактерной терапии зависит от наличия, выраженности и площади атрофии (необратимой утраты желез желудка с замещением их фиброзной тканью или метаплазированным эпителием) на момент эрадикации H. pylori. Максимальный профилактический эффект эрадикации H. pylori достигается при отсутствии атрофических изменений слизистой оболочки желудка, т. е. на стадии поверхностного гастрита [2, 3, 5–8].
Хронический гастрит, вызванный инфекцией Н. pylori, в том числе у больных с ее бессимптомным течением, можно рассматривать как показание к проведению эрадикационной терапии инфекции Н. pylori (УДД 1, УУР В).
Любой индивидуум может обратиться к врачу для диагностики Н. pylori и проведения лечения инфекции при положительном результате. Врач может посоветовать провести диагностику и лечение инфекции Н. pylori в профилактических целях, оценив наличие или отсутствие противопоказаний к антибиотикотерапии и дополнительных факторов риска развития рака желудка (например, злостное курение, отягощенный семейный анамнез, наличие предраковых изменений в желудке, таких как атрофия и кишечная метаплазия) [2, 8]. Таким образом будет проведено этиотропное лечение при хроническом гастрите и осуществлен оппортунистический скрининг гастрита как предракового заболевания. Повышенный риск развития аденокарциномы желудка в отдельных профессиональных популяциях и регионах нашей страны может служить основанием для осуществления организованного скрининга инфекции Н. pylori.
При хроническом гастрите, в том числе атрофическом, после окончания эрадикационной терапии возможно продолжение лечения препаратом висмута до 4–8 нед для обеспечения защиты слизистой оболочки желудка (УДД 5, УУР D) [8, 9].
Эрадикационную терапию Н. pylori желательно провести больным хроническим геликобактерным гастритом в случае назначения им ингибиторов протонной помпы (ИПП) на длительный срок (УДД 3, УУР C) [3]. В зависимости от модели колонизации слизистой оболочки желудка бактерией выделяют гастрит с поражением антрального отдела и пангастрит с преимущественным поражением тела желудка. Модель колонизации зависит от кислотности в желудке: при ее нормальных или повышенных значениях, как правило, развивается антральный гастрит. В случае снижения кислотности, в том числе при проведении антисекреторной терапии ИПП, происходит колонизация бактерией тела желудка параллельно с усилением воспаления и ускорением процесса атрофии слизистой оболочки в этом отделе. Эрадикация Н. pylori способствует излечению хронического гастрита и ликвидации его морфологических проявлений независимо от продолжения антисекреторной терапии [10–12].
Показанием к обязательному проведению эрадикационной терапии инфекции H. pylori служит язвенная болезнь (ЯБ) желудка и двенадцатиперстной кишки в стадии обострения и ремиссии (УДД 1, УУР А) [1, 13, 14]. При осложненных формах ЯБ, в первую очередь при кровотечении, эрадикационная терапия должна быть проведена обязательно и начата при переводе больного на пероральный прием лекарственных средств (УДД 1, УУР А) [1, 13].
Благодаря успешному проведению эрадикации стало реальным обсуждение вопроса о принципиальной излечимости ЯБ на основании данных с высокой степенью доказательности. Число больных, которых необходимо пролечить (number needed to treat) посредством проведения эрадикации H. pylori для предотвращения одного случая рецидива язвы двенадцатиперстной кишки, составило 2, для предотвращения рецидива язвы желудка — 3 [15]. Эрадикационная терапия также более эффективна для заживления язв любой локализации даже по сравнению с монотерапией антисекреторными средствами [15]. При осложненной ЯБ эрадикационная терапия инфекции H. pylori необходима для успешной профилактики повторных осложнений: так, число больных, которых необходимо пролечить посредством проведения эрадикации H. pylori для предотвращения одного случая повторного язвенного кровотечения, составило 5 [16].
Показанием к обязательному проведению эрадикационной терапии инфекции H. pylori служит MALT-лимфома желудка (УДД 1, УУР В) [3, 14, 17]. Антигеликобактерная терапия признана эффективным инициальным методом лечения локализованной MALT-лимфомы желудка у H. pylori-позитивных больных, которое может привести к регрессии опухоли и долговременному контролю над ней у большинства из них [17]. Оценка эффективности антигеликобактерной терапии и при необходимости назначение повторного курса лечения входят в алгоритм ведения больных с MALT-лимфомой желудка. Направление больного в специализированное онкологическое учреждения для дальнейшего наблюдения является обязательным.
Обязательно проведение эрадикационной терапии инфекции H. pylori больным, которым планируют выполнить эндоскопическую резекцию на стадии раннего рака желудка или она уже проведена (УДД 1, УУР А) [1, 14]. Эффективная антигеликобактерная терапия у данной категории пациентов служит надежной мерой профилактики метахронного рака желудка [18–20].
Гастропатия, индуцированная приемом нестероидных противовоспалительных средств (НПВС), служит основанием для обязательного проведения эрадикационной терапии инфекции H. pylori (УДД 1–2, УУР В). Инфекция H. pylori признана независимым фактором риска образования язв при приеме НПВС. Эрадикацию H. pylori обязательно назначают больным, при лечении которых планируют длительное применение НПВС и аспирина, а также пациентам с длительным анамнезом ЯБ, особенно при развитии ее осложнений [3, 21]. Антигеликобактерное лечение снижает риск возникновения неосложненных и осложненных гастродуоденальных язв при лечении НПВС и аспирином, в том числе при приеме последнего в низких дозах [22]. Однако проведение только эрадикации H. pylori полностью не исключает риск образования гастродуоденальных язв и их осложнений, в первую очередь кровотечений, у больных, уже принимающих НПВС [14, 23].
Функциональная диспепсия (ФД) является показанием к проведению эрадикационной терапии инфекции H. pylori (УДД 1, УУР В) [2, 24, 25]. При лечении больных хроническим гастритом с симптомами диспепсии она служит терапией первого выбора, позволяющей исключить из группы пациентов с ФД больных с диспепсией, ассоциированной с H. pylori, т. е. обусловленной именно этой инфекцией [2, 24]. Мета-анализ 17 исследований, включавший 3566 человек, показал исчезновение симптомов диспепсии после проведения антигеликобактерной терапии, при этом снижение относительного риска составило 10% (95% доверительный интервал — ДИ — 6–14%), а число больных, которых необходимо пролечить,— 14 (95% ДИ 10–25) [26].
Специального обсуждения требует вопрос о целесообразности проведения эрадикации H. pylori при гастроэзофагеальной рефлюксной болезни (ГЭРБ). Эрадикационная терапия инфекции H. pylori не входит в программу ведения пациентов с ГЭРБ и не отвечает целям лечения этого заболевания (например, целям купирования изжоги, заживления эрозий пищевода, профилактики рецидива ГЭРБ) [27]. Несмотря на то что в эпидемиологических исследованиях не установлена связь между выявлением H. pylori и развитием ГЭРБ, а также аденокарциномы пищевода, инфекцию H. pylori в этом случае не следует расценивать как защитный фактор [28–30]. В том случае, если проведение эрадикационной терапии инфекции H. pylori необходимо по другим показаниям (ЯБ, хронический геликобактерный гастрит), такая терапия может быть проведена при ГЭРБ, поскольку она не провоцирует ухудшение ее течения и не оказывает влияния на эффективность лечения [31–33].
Назначение эрадикационной терапии инфекции H. pylori признано целесообразным при аутоиммунной тромбоцитопении (УДД 1, УУР В) [1, 3, 14] и железодефицитной анемии (УДД 1, УУР В) [1, 3, 14]. Систематический обзор, включавший 25 исследований (1555 взрослых пациентов), продемонстрировал тенденцию к увеличению количества тромбоцитов после уничтожения H. pylori [34]. У H. pylori-позитивных лиц железодефицитная анемия развивается достоверно чаще, чем у неинфицированных. Согласно результатам мета-анализа 7 исследований, после проведения эрадикационной терапии инфекции H. pylori в сочетании с приемом препаратов железа отмечен более высокий уровень ферритина (но не гемоглобина) по сравнению с таковым при назначении только препаратов железа [35].
Диагностика
Диагностика инфекции H. pylori
Референсными методами диагностики инфекции H. pylori служат дыхательный тест с мочевиной, меченной 13С, и определение антигена H. pylori в кале лабораторным способом (УДД 2, УУР В) [1, 3, 36].
В качестве метода первичной диагностики у лиц, у которых имеются показания к проведению эзофагогастродуоденоскопии, может быть использован быстрый уреазный тест с получением биоптата из антрального отдела и тела желудка (УДД 4, УУР С) [3, 13, 37, 38].
Необходимо учитывать, что при лечении с применением ИПП могу быть получены ложноотрицательные результаты диагностических тестов [39], поэтому рекомендуется отменить ИПП не менее чем за 2 нед до проведения диагностических мероприятий [40]. Антибиотики и препараты висмута следует отменить не менее чем за 4 нед до выполнения диагностических тестов.
Серологические методы определения антител к H. pylori могут быть назначены в качестве первичной диагностики инфекции, в том числе в случае снижения степени колонизации бактерией слизистой оболочки желудка, например после недавнего приема антисекреторных или антибактериальных лекарственных средств, при язвенном кровотечении, атрофическом гастрите (УДД 3, УУР С) [3, 41].
Оценка эффективности эрадикационной терапии инфекции H. pylori
Оценку необходимо осуществлять с помощью дыхательного теста с мочевиной, меченной 13С, или определения антигена H. pylori в кале лабораторным способом не ранее чем через 4 недпосле окончания курса антигеликобактерной терапии либо после окончания лечения сопутствующих заболеваний любыми антибиотиками, препаратом висмута или антисекреторными средствами (УДД 2, УУР В) [1, 3, 42–44]. Серологические методы определения антител к H. pylori в этой ситуации не применяют (УДД 2, УУР В).
В отсутствие возможности использовать референсные методы диагностики целесообразно комбинировать доступные диагностические тесты или (в случае применения методов непосредственного обнаружения бактерии в биоптате слизистой оболочки желудка — бактериологического, морфологического, быстрого уреазного теста) исследовать хотя бы два биоптата из тела желудка и один биоптат из антрального отдела (УДД 5, УУР D).
Лечение
Лечение больных с инфекцией H. pylori
Антибиотикорезистентность считают основной причиной неэффективности эрадикации H. pylori [45, 46]. Для выбора режимов антигеликобактерной терапии в консенсусе Маастрихт V EHMSG на основании данных локальных эпидемиологических исследований по определению чувствительности штаммов H. pylori к антимикробным препаратам in vitro эмпирически установлено пороговое значение резистентности к кларитромицину 15% [3]. Клиническое значение имеет резистентность H. pylori к кларитромицину, метронидазолу и левофлоксацину. Можно прогнозировать индивидуальный результат применения любого режима терапии в случае известной эффективности его при наличии чувствительного или резистентного штамма, а также известных уровней антибиотикорезистентности в конкретной популяции. Важно отметить, что антибиотикорезистентность характеризует определенную популяцию в определенном географическом регионе [3].
На заседании Экспертного совета РГА 19 мая 2017 г. академик РАН В.Т. Ивашкин подчеркнул, что полученные in vitro показатели антибиотикорезистентности следует крайне осторожно интерпретировать при оценке эффекта многокомпонентной антигеликобактерной терапии, в том числе включающей ИПП, существенно изменяющей рН желудка и жизнедеятельность бактерии [4]. Влияние рН желудка на чувствительность штаммов H. pylori к антибактериальным препаратам не изучено [4]. Особенности назначаемой схемы эрадикационной терапии, такие как выбор лекарственных препаратов, в частности антисекреторных, дозы и частоты приема в течение дня, в том числе в зависимости от приема пищи, конкретной лекарственной формы, продолжительности лечения, обусловливают успех терапии [4, 47–49]. Недоступность данных по антибиотикорезистентности H. pylori в конкретном регионе не является основанием для отказа от проведения антигеликобактерной терапии, так как выбор лечебной тактики основан на эмпирической оптимизации любого режима.
Суммируя результаты российских исследований, можно сделать заключение, что средний уровень резистентности 650 штаммов H. pylori, выявленных в различных регионах России за последние 10 лет, к кларитромицину составил 8,3%, к метронидазолу — 35,8%. Эти показатели свидетельствуют о низком уровне резистентности H. pylori к кларитромицину и метронидазолу в большинстве регионов России. Распространенность штаммов H. pylori с двойной устойчивостью к кларитромицину и метронидазолу низкая — в среднем 3,3% [4, 50–54]. Таким образом, с одной стороны, в Российской Федерации большинство доступных данных по-прежнему свидетельствует о низкой резистентности H. pylori к кларитромицину (менее 15%), с другой стороны, уровни антибиотикорезистентности неизвестны в большинстве регионов.
Терапия первой линии
Терапией первой линии для эрадикации H. pylori служит стандартная тройная терапия, включающая ИПП (в стандартной дозе 2 раза в сутки), кларитромицин (500 мг 2 раза в сутки) и амоксициллин (1000 мг 2 раза в сутки) (УДД 1, УУР 1). Стандартную тройную терапию следует назначать, применяя различные меры, повышающие ее эффективность (см. далее).
Как альтернативный вариант эрадикационной терапии первой линии может быть назначена классическая четырехкомпонентная терапия на основе висмута трикалия дицитрата (120 мг 4 раза в сутки) в сочетании с ИПП (в стандартной дозе 2 раза в сутки), тетрациклином (500 мг 4 раза в сутки) и метронидазолом (500 мг 3 раза в сутки) (УДД 1, УУР A). Другой альтернативный вариант эрадикационной терапии первой линии — квадротерапия без препарата висмута, которая включает ИПП (в стандартной дозе 2 раза в сутки), амоксициллин (1000 мг 2 раза в сутки), кларитромицин (500 мг 2 раза в сутки) и метронидазол (500 мг 3 раза в сутки) (УДД 2, УУР В).
Классическая квадротерапия с препаратом висмута продолжает демонстрировать высокую эффективность в современных условиях, в том числе при доказанной резистентности H. pylori к метронидазолу [3, 55–57]. Эту схему лечения применяют и как альтернативную терапию первой линии, и как терапию второй линии после применения стандартной тройной терапии с кларитромицином. Квадротерапия без препарата висмута, или сочетанная терапия (по-английски «concomitant»), включающая ИПП и сочетание амоксициллина, кларитромицина и метронидазола, в последние годы в международных и национальных рекомендациях уверенно занимает место терапии первой линии, особенно в регионах с высокой резистентностью к кларитромицину [3, 58]. По сути сочетанная терапия является стандартной тройной схемой, усиленной метронидазолом.
Меры, повышающие эффективность эрадикационной терапии инфекции H. pylori
В «Рекомендациях Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции H. pylori у взрослых» редакции 2012 г. перечислены меры, повышающие эффективность эрадикационной терапии [1]. За последние годы в литературе сформировалось четкое представление о путях оптимизации антигеликобактерного лечения [49, 56–60]. Очевидно, что эти меры должны быть универсальными и могут быть применены в любой линии терапии, а комбинирование этих мер позволяет добиться наилучшего результата у конкретного пациента.
Продолжительность лечения
Продолжительность всех схем лечения H. pylori должна составлять 14 дней, минимальная продолжительность 10 дней может быть назначена в тех случаях, если исследования, проведенные в данном регионе, подтвердили ее высокую эффективность Увеличение продолжительности лечения имеет универсальный характер, так как положительный эффект наблюдается при использовании всех изученных режимов антигеликобактерного лечения, в том числе при стандартной тройной терапии (УДД 1, УУР 1) [3, 49, 56–60].
Кохрейновский мета-анализ 45 рандомизированных контролируемых исследований (РКИ) в параллельных группах однозначно показывает повышение частоты случаев эрадикации H. pylori в результате проведения тройной терапии при увеличении ее продолжительности с 7 до 14 дней (72,9% против 81,9%), при этом относительный риск (RR) персистенции H. pylori составляет 0,66 (95%ДИ 0,60–0,74), NNT — 11 (95%ДИ 9–14). Выраженный эффект наблюдали при сочетании ИПП с кларитромицином и амоксициллином (34 исследования, RR0,65, 95%ДИ 0,57–0,75; NNT 12, 95%ДИ 9–16), а также ИПП с левофлоксацином и амоксициллином (2 исследования, RR0,37, 95%ДИ 0,16–0,83; NNT 3, 95%ДИ 2–10). Значимое повышение эффективности эрадикации H. pylori отмечено при увеличении продолжительности тройной терапии с 7 до 10 дней (24 исследования, 75,7% против 79,9%; RR0,80, 95%ДИ 0,72–0,89; NNT 21, 95%ДИ 15–38) и с 10 до 14 дней (12 исследований, 78,5% против 84,4%; RR0,72, 95%ДИ 0,58–0,90; NNT 17, 95%ДИ 11–46), особенно для сочетания ИПП с кларитромицином и амоксициллином при увеличении продолжительности с 7 до 10 дней (17 исследований, RR0,80, 95%ДИ 0,70–0,91) и с 10 до 14 дней (10 исследований, RR0,69, 95%ДИ 0,52–0,91) [61].
В основе увеличения продолжительности квадротерапии с висмута трикалия дицитратом лежат данные о преодолении резистентности к метронидазолу в итоге такого лечения. В Китае при резистентноcти H. pylori к метронидазолу более чем в 40% случаев квадротерапия продолжительностью 7 дней была неэффективной [62], в то время как при проведении ее в течение 10 дней, а особенно 2 нед всегда удавалось достичь заданного уровня эрадикации H. pylori даже при высокой резистентности к метронидазолу [63, 64]. Эффективность квадротерапии без препарата висмута также возрастает при увеличении ее продолжительности [3, 60].
Выбор ИПП и его дозы как основы эрадикационной терапии инфекции H. pylori
Схемы эрадикационной терапии обязательно включают ИПП. В составе эрадикационной терапии их применяют в следующих дозах: лансопразол 30 мг 2 раза в сутки, омепразол 20 мг 2 раза в сутки, пантопразол 40 мг 2 раза в сутки, рабепразол 20 мг 2 раза в сутки или эзомепразол 20 мг 2 раза в сутки (УДД 1, УУР 1) [1, 3]. Применение ИПП в высокой дозе (удвоенной по сравнению со стандартной) способствует повышению эффективности лечения (УДД 1, УУР D) [1, 3, 65, 66].
При проведении эрадикационной терапии предпочтение отдают рабепразолу и эзомепразолу (УДД 1, УУР 1) [3, 67].
Рабепразол — современный стандарт терапии кислотозависимых заболеваний, включая эрадикационную терапию инфекции Н. pylori. Согласно данным мета-анализов, благодаря выраженному кислотоподавляющему эффекту рабепразол в составе эрадикационой терапии обеспечивает лучшие показатели эрадикации H. pylori по сравнению с более ранними ИПП (омепразол, лансопразол, пантопразол). Рабепразол отличается от других ИПП минимальной зависимостью от фенотипически детерминированных вариантов печеночного метаболизма, давая более предсказуемый антисекреторный эффект, так как он, в отличие от других ИПП, метаболизируется преимущественно в результате неферментативного процесса [68, 69]. Это служит обоснованием его предпочтительного использования в странах Европейского региона (в том числе в России), в которых высока распространенность фенотипа быстрых метаболизаторов [70–72]. При этом у рабепразола выявлены специальные характеристики (собственный антигеликобактерный эффект, стимуляция секреции муцинов в слизистой оболочке желудка), которые могут обеспечивать дополнительные преимущества при эрадикациии H. pylori [73–76].
Согласно данным мета-анализов, выраженное антисекреторное действие эзомепразола в составе эрадикационной терапии инфекции H. pylori обеспечивает более высокую эффективность лечения по сравнению с таковой при использовании омепразола, лансопразола и пантопразола [67]. Эзомепразол представляет собой S-энантиомер (левый изомер) омепразола и благодаря стереоселективным особенностям взаимодействия с цитохромом P450 в печени обладает большей биодоступностью, чем омепразол, следствием чего является более предсказуемый контроль секреции кислоты в желудке, который не зависит от индивидуальных особенностей лекарственного метаболизма у лиц, принимающих ИПП [77].
Включение висмута трикалия дицитрата в состав эрадикационной терапии инфекции H. pylori
Добавление к стандартной тройной терапии висмута трикалия дицитрата в дозе 240 мг 2 раза в сутки или 120 мг 4 раза в сутки служит мерой повышения ее эффективности (УДД 2, УУР B) [1, 8], которая основана на бактерицидном эффекте висмута трикалия дицитрата по отношению к H. pylori, а также цитопротективных свойствах этой соли висмута [78–80]. Антигеликобактерную активность солей висмута впервые описал B.J. Marshall: при электронной микроскопии было показано, что уже через 30–90 мин после приема лекарственного средства внутрь бактерии отделялись от эпителиоцитов желудка (блокирование адгезии) и демонстрировали признаки структурной деградации из-за появления депозитов висмута на поверхности и внутри микроорганизмов [85]. Недавно было установлено, что висмута трикалия дицитрат затрудняет проникновение протонов внутрь бактерии, сохраняя рН цитоплазмы в пределах, благоприятных для максимальной метаболической активности микроорганизма, что делает ее уязвимой для антибиотиков [86].
Данные российских исследований по изучению результатов добавления висмута трикалия дицитрата к эрадикационной терапии инфекции H. pylori раскрывают потенциал такого подхода и показывают, что эта мера оптимизации эффективна и для тройной, и для последовательной схем лечения [87–90]. Некоторые клинические исследования, в которых был достигнут высокий уровень эрадикации H. pylori при использовании висмута трикалия дицитрата, выполнены с оценкой чувствительности микроорганизма в данном регионе, причем эта мера повышает эффективность терапии на 30–40% при наличии антибиотикорезистентности к кларитромицину и левофлоксацину [91–95].
Добавление препарата висмута к тройной терапии инфекции H. pylori является общепризнанной практикой в Китае [96], а в последние годы эта мера стала находить поддержку в Европе и США [60, 80]. Такая мера оптимизации усиливает эффект антибиотиков, препятствует развитию антибиотикорезистентности, особенно с учетом того, что резистентность H. pylori к висмута трикалия дицитрату не формируется [60, 80]. Мета-анализ 35 РКИ, включавших 4763 пациента, показал безопасность висмута трикалия дицитрата и хорошую переносимость такого лечения больными [97].
Включение пробиотика в состав эрадикационной терапии инфекции H. pylori
Включение пробиотиков, в том числе комбинированного пробиотика, содержащего Bifidobacterium bifidum, B. longum, B. infantis, Lactobacillus rhamnosus, в состав эрадикационной терапии инфекции H. pylori приводит к повышению ее эффективности и снижению частоты возникновения нежелательных явлений, включая развитие C.difficile-ассоциированной болезни (УДД 1, УУР B) [3, 8, 102–107].
Механизм действия пробиотиков на инфекцию H. pylori и их синергизма с эрадикационной терапией полностью не раскрыт. Снижение колонизационной способности H. pylori при наличии пробиотиков показано в эксперименте. Предполагают, что пробиотические штаммы способствуют блокаде уреазы H. pylori, снижению адгезии H. pylori к желудочным эпителиоцитам (доказано для Lactobacillus) и подвижности H. pylori [94, 100].
В большинстве систематических обзоров и мета-анализов сообщается об эффективности применения пробиотиков в сочетании с эрадикационной терапией H. pylori в отношении увеличения процента эрадикации [102–107]. Так, в мета-анализе Z. Lv и соавт. [102] по итогам оценки 21 РКИ с числом больных 3814 уровень эрадикации H. pylori при использовании пробиотиков составил 80,3% по сравнению с 72,2% при проведении терапии без пробиотиков (RR1,12, 95%ДИ 1,06–1,19). Положительное влияние на эффективность лечения оказывали применение пробиотиков в течение более 2 нед, назначение мультиштаммовых пробиотиков и Lactobacillus [102]. При добавлении пробиотиков к эрадикационной терапии инфекции H. pylori снижается частота возникновения нежелательных явлений, наблюдающихся при ее проведении [102–107], например, по данным Z. Lv и соавт. [102], RR составил 0,60 (95%ДИ 0,40–0,91).
Несмотря на значительное количество исследований, посвященных изучению эффективности и безопасности пробиотиков, количество используемых бактериальных штаммов, дозы препаратов и продолжительность лечения существенно варьируют. Очевидна необходимость дальнейшего поиска наиболее эффективной комбинации бактериальных штаммов и оптимальной длительности проводимого лечения, оценки состояния кишечной микрофлоры до и после окончания терапии. В консенсусе Маастрихт V EHMSG отмечено, что определенные пробиотики могут оказывать положительное влияние на эрадикацию H. pylori, а также снижают частоту возникновения нежелательных явлений со стороны желудочно-кишечного тракта, вызываемые антигеликобактерным лечением. Определенные штаммы должны быть отобраны на основе доказанной клинической эффективности [3].
Эффективность отечественного пробиотического препарата, содержащего наиболее распространенных представителей нормальной кишечной микрофлоры (B. bifidum, B. longum, B. infantis, L. rhamnosus), изучена в отечественных исследованиях, в которых отмечены улучшение показателей качества жизни, устранение синдрома избыточного бактериального роста (по данным водородного дыхательного теста), предотвращение развития C. difficile-ассоциированной болезни [108–110].
Включение ребамипида в состав эрадикационной терапии инфекции H. pylori
Включение ребамипида в дозе 100 мг 3 раза в сутки в состав эрадикационной терапии инфекции H. pylori приводит к повышению ее эффективности (УДД 1, УУР B) [116]. Защитные свойства ребамипида позволяют рекомендовать его не только для проведения курса эрадикационной терапии инфекции H. pylori, но и для продолжения лечения, особенно при эрозивноязвенных поражениях желудка и двенадцатиперстной кишки (УДД 1, УУР B) [116, 117]. Продолжительность курса постэрадикационной терапии ребамипидом составляет 4–8 нед.
Ребамипид обеспечивает защиту слизистой оболочки желудочно-кишечного тракта благодаря стимулированию синтеза простагландинов и ингибированию продуктов окислительного стресса, провоспалительных цитокинов и хемокинов. Препарат способствует улучшению кровоснабжения слизистой оболочки желудка, повышает синтез гликопротеинов и бикарбонатов, усиливает пролиферацию эпителиальных клеток желудка [111, 112]. Собственный антигеликобактерный эффект ребамипида нуждается в дальнейшем изучении, но снижение адгезии H. pylori к эпителиоцитам в культуре клеток при его воздействии доказано [113]. Длительный прием ребамипида (в течение 12 мес) приводит к регрессу морфологических признаков гастрита со снижением нейтрофильной и мононуклеарной инфильтрации как в присутствии H. pylori, так и после эрадикации инфекции [114, 115].
Потенциальный антигеликобактерный эффект ребамипида подтвержден в ходе клинических исследований, в которых оценивали эффективность препарата в рамках схем эрадикационной терапии. Недавно проведенный мета-анализ 6 РКИ (611 пациентов) продемонстрировал эффективность ребамипида при включении его в состав эрадикационной терапии: 73,3% против 61,4%. Отношение шансов (ОШ) успешной эрадикации при сочетанном назначении ребамипида составило 1,74 (95%ДИ 1,19–2,53), а достоверных различий в частоте развития побочных эффектов в обеих группах не выявлено (ОШ 0,69; 95%ДИ 0,376–1,300; р=0,329) [116]. Группа исследователей проанализировали эффективность лечения ребамипидом после окончания эрадикационной терапии. В РКИ, включавшем 309 пациентов, которые завершили курс антигеликобактерного лечения, частота рубцевания язвенного дефекта слизистой оболочки желудка в группе больных, продолжавших принимать ребамипид, оказалась выше, чем в группе больных, получавших плацебо (80% против 66,1%) [117]. Таким образом, препарат может быть использован для продолжения лечения и после окончания эрадикационной терапии, поскольку он потенцирует репаративные процессы в слизистой оболочке желудка.
Повышение приверженности пациентов эрадикационной терапии инфекции H. pylori
Подробное инструктирование пациентов и контроль за точным соблюдением назначенного режима приема лекарственных средств повышают их приверженность лечению и эффективность эрадикационной терапии.
Приверженность пациентов лечению рассматривают как важнейший фактор эффективности эрадикационной терапии инфекции H. pylori, причем отсутствие комплаентности может быть причиной неудачи при наличии чувствительных к назначенным антибиотикам штаммов H. pylori и развития антибиотикорезистентности [1, 3, 118]. Согласно классическим данным D.Y. Graham и соавт. (1992), эффективность эрадикации H. pylori у пациентов, которые приняли более 60% предписанных лекарственных средств, соответствовала результатам двухнедельного курса с включением тетрациклина и препарата висмута и составила 96%, а у пациентов, нарушавших режим лечения, — лишь 69% [119]. Традиционно считается, что комплаентность определяет ряд факторов: сложность многокомпонентного лечения, его продолжительность и эффективность, возникновение нежелательных явлений, мотивация врача и пациента, полнота информирования больного [118].
Может создаться впечатление, что современная тенденция к переходу от трех к четырем препаратам в составе терапии может оказать негативное влияние на приверженность лечению. Однако результаты ряда оригинальных исследований, обзоров и мета-анализов свидетельствуют о том, что комплаентность не зависит от назначаемого режима терапии, в том числе от количества таблеток, которое следует принять в течение суток. L.A. Fischbach и соавт. [120] при проведении мета-анализа не выявили уменьшения приверженности лечению при назначении четырехкомпонентной терапии по сравнению с таковой при тройной терапии. Современную квадротерапию с висмутом разрабатывали с учетом улучшения комплаентности [121].
Мета-анализ многокомпонентных схем приводит высокие данные по комплаентности: для исследований, в которых сравнивали гибридную схему лечения (чередование двойной терапии и квадротерапии без препарата висмута) с последовательной, комплаентность составила 96 и 98%, для исследований, в которых проводили сравнительную оценку гибридной и сочетанной схем,— 95,8 и 93,2% соответственно [122]. Добавление пробиотика к эрадикационной терапии инфекции H. pylori не оказывает отрицательного влияния на приверженность терапии (RR0,98; 95%ДИ 0,68–1,39; p=0,889) [105].
Индивидуальная работа с пациентом, создание у него правильной мотивации, предоставление полной информации о лечении и контроль за его соблюдением — лучшие методы повышения приверженности антигеликобактерной терапии. Благодаря таким простым мерам, как объяснение включенным в исследование больным природы их заболевания, особенностей лечения, возможных нежелательных явлений, предоставление листовки с этой информацией и дневника приема лекарственных препаратов, телефонный звонок с напоминанием о необходимости соблюдения режима терапии, удалось увеличить эффективность H. pylori до 94,7% (против 73,7%) и комплаентность до 92,1% (против 23,7% в группе больных с рутинным назначением терапии) [123].
Терапия второй и третьей линий
Квадротерапию с висмута трикалия дицитратом применяют как основную схему терапии второй линии при неэффективности стандартной тройной терапии (УДД 1, УУР 1) [1, 3]. Другая схема терапии второй линии включает ИПП (в стандартной дозе 2 раза в сутки), левофлоксацин (500 мг 2 раза в сутки) и амоксициллин (1000 мг 2 раза в сутки) (УДД 2, УУР В) [1, 3]. Тройная терапия с левофлоксацином может быть назначена только гастроэнтерологом по строгим показаниям. Терапию третьей линии подбирают индивидуально в зависимости от выбора предшествующих схем лечения, по возможности основываясь на результатах определения чувствительности H. pylori к антибиотикам.
Информация
Источники и литература
-
Клинические рекомендации Российской гастроэнтерологической ассоциации
- 1. Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин
А.А. и комитет экспертов. Рекомендации Российской
гастроэнтерологической ассоциации по диагности-
ке и лечению инфекции Helicobacter pylori у взрослых.
Рос журн гастроэнтерол гепатол колопроктол 2012;
22(1):87-9 [Ivashkin V.T., Mayev I.V., Lapina T.L.,
Sheptulin A.A. and expert board. Diagnostics and
treatment of Helicobacter pylori infection in in adults:
guidelines of the Russian gastroenterological Association.
Ross z gastroenterol gepatol koloproktol 2012; 22(1):
87-9].
2. Sugano K., Tack J., Kuipers E.J. et al. Kyoto global
consensus report on Helicobacter pylori gastritis. Gut
2015;64:1353-67.
3. Malfertheiner P., Megraud F., O’Morain C.A.,
Gisbert J.P., Kuipers E.J. et al. Management of
Helicobacter pylori infection — the Maastricht V/
Florence Consensus Report. Gut 2017;66:6-30.
4. Ивашкин В.Т., Маев И.В., Лапина Т.Л.,
Шептулин А.А., Трухманов А.С., Абдулхаков Р.А.,
Алексеенко С.А., Дехнич Н.Н., Козлов Р.С.,
Кляритская И.Л., Курилович С.А., Осипенко М.Ф.,
Симаненков В.И., Хлынов И.Б. Лечение инфекции
Helicobacter pylori: мейнстрим и новации (Обзор лите-
ратуры и резолюция Экспертного совета Российской
гастроэнтерологической ассоциации, 19 мая 2017 г.). Рос
журн гастроэнтерол гепатол колопроктол 2017; 27(4):4-
21 [Ivashkin V.T., Mayev I.V., Lapina T.L., Sheptulin
A.A., Trukhmanov A.S., Abdulkhakov R.A., Alekseyenko
S.A., Dekhnich N.N., Kozlov R.S., Klyaritskaya I.L.,
Kurilovich S.A., Osipenko M.F., Simanenkov V.I.,
Khlynov I.B. Treatment of Helicobacter pylori infection:
mainstream and innovations (Review of literature
and resolution of Advisory council of the Russian
gastroenterological association, May 19, 2017). Ross z
gastroenterol gepatol koloproktol 2017; 27(4):4-21].
5. IARC Helicobacter pylori Working Group (2014).
Helicobacter pylori Eradication as a Strategy for
Preventing Gastric Cancer. Lyon, France: International
Agency for Research on Cancer (IARC Working Group
Reports, No.http://www.iarc.fr/en/publications/
pdfs-online/wrk/wrk8/index.php
6. Ford A.C., Forman D., Hunt R.H., Yuan Y.,
Moayyedi P. Helicobacter pylori eradication therapy to
prevent gastric cancer in healthy asymptomatic infected
individuals: systematic review and meta-analysis of
randomised controlled trials. Br Med J 2014;348: g3174.
7. Seta T., Takahashi Y., Noguchi Y., Shikata S.,
Sakai T., Sakai K. et al. Effectiveness of Helicobacter
pylori eradication in the prevention of primary gastric
cancer in healthy asymptomatic people: A systematic
review and meta-analysis comparing risk ratio with risk
difference. PLoS ONE2017;12(8): e0183321.
8. Ивашкин В.Т., Лапина Т.Л., Шептулин А.А.,
Трухманов А.С. и др. Практические шаги по про-
филактике рака желудка в Российской Федерации:
алгоритм ведения пациентов с хроническим гелико-
бактерным гастритом (Материалы и резолюция совета
экспертов, 9 декабря 2013 г.). Рос журн гастроэнтерол
гепатол колопроктол 2014; 24 (2):102-4 [Ivashkin V.T.,
Lapina T.L., Sheptulin A.A., Trukhmanov A.S. et
al. Practical steps on stomach cancer prevention in the
Russian Federation: algorithm for chronic H.pyloriassociated
gastritis management (Proceedings and the
resolution of the expert board, December 9, 2013). Ross
z gastroenterol gepatol koloproktol 2014; 24 (2):102-4.].
9. Кононов А.В., Мозговой С.И., Рыбкина Л.Б.,
Бунова С.С., Шиманская А.Г. Оценка цитопротективного влияния висмута трикалия дицитрата на сли-
зистую оболочку желудка при эрадикации H. pylori
и пролонгированном приеме препарата. Рос журн
гастроэнтерол гепатол колопроктол 2006; 16(6):21-
8 [Kononov A.V., Mozgovoy S.I., Rybkina L.B.,
Bunova S.S., Shimanskaya A.G. Estimation of bismuth
tripotassium dicitrate cytoprotective effect on stomach
mucosa at H. pylori eradication and prolonged drug
administration. Ross z gastroenterol gepatol koloproktol
2006; 16(6):21-8].
10. Kuipers E.J., Uyterlinde A.M., Peña A.S. et al.
Increase of Helicobacter pylori-associated corpus gastritis
during acid suppressive therapy: implications for longterm
safety. Am J Gastroenterol 1995;90:1401-6.
11. Schenk B.E., Kuipers E.J., Nelis G.F. et al. Effect of
Helicobacter pylori eradication on chronic gastritis during
omeprazole therapy. Gut 2000;46:615-21.
12. Kuipers E.J., Nelis G.F., Klinkenberg-Knol E.C. et al.
Cure of Helicobacter pylori infection in patients with reflux
oesophagitis treated with long term omeprazole reverses
gastritis without exacerbation of reflux disease: results of a
randomised controlled trial. Gut 2004;53:12-20.
13. Ивашкин В.Т., Шептулин А.А., Маев И.В.,
Баранская Е.К., Трухманов А.С., Лапина Т.Л.,
Бурков С.Г., Калинин А.В., Ткачев А.В. Клинические
рекомендации Российской гастроэнтерологической ассо-
циации по диагностике и лечению язвенной болез-
ни. Рос журн гастроэнтерол гепатол колопроктол
2016; 26(6):40-54. DOI:10.22416/1382-4376-2016-6-32-
39 [Ivashkin V.T., Sheptulin A.A., Mayev I.V.,
Baranskaya Ye.K., Trukhmanov A.S., Lapina T.L.,
Burkov S.G., Kalinin A.V., Tkachev A.V. Diagnostics
and treatment of peptic ulcer disease: clinical guidelines
of the Russian gastroenterological Association. Ross z
gastroenterol gepatol koloproktol 2016; 26(6):40-54.
DOI: 10.22416/1382-4376-2016-6-32-39].
14. Chey W.D., Leontiadis G.I., Howden C.W., Moss S.F.
ACG Clinical Guideline: treatment of Helicobacter
pylori infection. Am J Gastroenterol 2017;112(2):212-39.
15. Ford A.C., Gurusamy K.S., Delaney B., Forman D.,
Moayyedi P. Eradication therapy for peptic ulcer disease
in Helicobacter pylori-positive people. Cochrane Database
Syst Rev 2016;4: CD003840. doi: 10.1002/14651858.
CD003840.pub5.
16. Gisbert J.P., Khorrami S., Carballo F., Calvet X.,
Gene E., Dominguez-Muñoz E. Meta-analysis:
Helicobacter pylori eradication therapy vs. antisecretory
non-eradication therapy for the prevention of recurrent
bleeding from peptic ulcer. Aliment Pharmacol Ther
2004;19(6):617-29.
17. Zucca E., Copie-Bergman C., Ricardi U.,
Thieblemont C., Raderer M., Ladetto M. Gastric
marginal zone lymphoma of MALT type: ESMO Clinical
Practice Guidelines for diagnosis, treatment and followup.
Ann Oncol 2013; 24 (Suppl 6): vi144-vi148.
18. Bang C.S., Baik G.H., Shin I.S. et al. Helicobacter
pylori eradication for prevention of metachronous
recurrence after endoscopic resection of early gastric
cancer. J Korean Med Sci 2015;30:749-56.
19. Jung, da H., Kim J.H., Chung H.S. et al. Helicobacter
pylori eradication on the prevention of metachronous
lesions after endoscopic resection of gastric neoplasm: a
meta-analysis. PLoS One 2015; 10:e0124725.
20. Yoon S.B., Park J.M., Lim C.H. et al. Effect of
Helicobacter pylori eradication on metachronous gastric
cancer after endoscopic resection of gastric tumors: a
meta-analysis. Helicobacter 2014;19:243-8.
- 1. Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин
Информация
В.Т. Ивашкин1, И.В. Маев2, Т.Л. Лапина1, А.А. Шептулин1, А.С. Трухманов1, Е.К. Баранская1, Р.А. Абдулхаков3, О.П. Алексеева4, С.А. Алексеенко5, Н.Н. Дехнич6, Р.С. Козлов7, И.Л. Кляритская8, Н.В. Корочанская9, С.А. Курилович10,11, М.Ф. Осипенко11, В.И. Симаненков12, А.В. Ткачев13, И.Б. Хлынов14, В.В. Цуканов15
1ФГАОУ ВО «Первый Московский государственный медицинский университет им. И.М. Сеченова» (Сеченовский университет) Минздрава России, г. Москва, Российская Федерация
2ФГБОУ ВО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Минздрава России, г. Москва, Российская Федерация
3ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России, г. Казань, Российская Федерация
4ГБУЗ «Нижегородская областная клиническая больница им. Н.А. Семашко» Минздрава Нижегородской области, г. Нижний Новгород, Российская Федерация
5ФГБОУ ВО «Дальневосточный государственный медицинский университет» Минздрава России, г. Хабаровск, Российская Федерация
6 ФГБОУ ВО «Смоленский государственный медицинский университет» Минздрава РФ, Кафедра факультетской терапии, г. Смоленск, Российская Федерация
7Научно-исследовательский институт антимикробной химиотерапии ФГБОУ ВО «Смоленский государственный медицинский университет» Минздрава РФ, г. Смоленск, Российская Федерация
8Медицинская академия им. С.И. Георгиевского ФГАОУ ВО «Крымский федеральный университет им. В.И. Вернадского», г. Симферополь, Российская Федерация
9ФГБОУ ВО «Кубанский государственный медицинский университет», ГБУЗ «Краевая клиническая больница № 2» Минздрава Краснодарского края, г. Краснодар, Российская Федерация
10Научно-исследовательский институт терапии и профилактической медицины — филиал ФГБНУ «Федеральный исследовательский центр Институт цитологии и генетики Сибирского отделения Российской академии наук» г. Новосибирск, Российская Федерация
11ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России, г. Новосибирск, Российская Федерация
12ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, г. Санкт-Петербург, Российская Федерация
13ФГБОУ ВО «Ростовский государственный медицинский университет», г. Ростов-на-Дону, Российская Федерация
14ФГБОУ ВО «Уральский государственный медицинский университет» Минздрава России, г. Екатеринбург, Российская Федерация
15ФИЦ КНЦ СО РАН, НИИ медицинских проблем Севера, г. Красноярск, Российская Федерация
Цель публикации. Ознакомить практикующих врачей с показаниями к проведению антигеликобактерной терапии, методами и порядком проведения диагностики и эрадикационной терапии инфекции Helicobacter pylori (H. pylori).
Основные положения. Хронический гастрит, вызванный инфекцией Н. pylori, в том числе у «бессимптомных» лиц, можно рассматривать как показание к проведению эрадикационной терапии инфекции Н. pylori в качестве этиотропного лечения и оппортунистического скрининга для профилактики рака желудка. Показаниями к обязательному проведению антигеликобактерной терапии служат язвенная болезнь желудка и двенадцатиперстной кишки, MALT-лимфома желудка, ранний рак желудка с эндоскопической резекцией. В качестве методов первичной диагностики инфекции H. pylori используют дыхательный тест с мочевиной, меченной 13С, определение антигена H. pylori в кале лабораторным способом, быстрый уреазный тест и серологический метод. После проведения антигеликобактерной терапии серологический метод не применяют. Согласно результатам большинства региональных исследований, показатели устойчивости штаммов H. pylori к кларитромицину в России не выше 15%. Получены данные об отсутствии высокой устойчивости H. pylori к метронидазолу и о низком уровне двойной устойчивости к кларитромицину и метронидазолу.
Терапией первой линии для эрадикации инфекции H. pylori служит стандартная тройная терапия, включающая ингибитор протонной помпы (ИПП), кларитромицин и амоксициллин. Стандартную тройную терапию следует проводить, применяя различные меры, повышающие ее эффективность. В качестве альтернативного варианта эрадикационной терапии первой линии может быть использована классическая четырехкомпонентная терапия на основе висмута трикалия дицитрата или квадротерапия без препаратов висмута, которая включает ИПП, амоксициллин, кларитромицин и метронидазол.
Квадротерапию с висмута трикалия дицитратом применяют также как основную схему терапии второй линии при неэффективности стандартной тройной терапии. Другая схема терапии второй линии включает ИПП, левофлоксацин и амоксициллин. Тройная терапия с левофлоксацином может быть назначена только гастроэнтерологом по строгим показаниям. Терапию третьей линии подбирают индивидуально в зависимости от выбора предшествующих схем лечения. Среди методов оптимизации, позволяющих повысить эффективность эрадикационной терапии инфекции H. pylori, следует отметить увеличение продолжительности лечения до 14 дней, выбор более современного ИПП или увеличение дозы ИПП, добавление висмута трикалия дицитрата или пробиотика.
Заключение. В каждом случае обнаружения H. pylori целесообразно решить вопрос о проведении эрадикационной терапии, что особенно актуально в связи с признанием эрадикации инфекции H. pylori эффективной мерой профилактики рака желудка. Методы оптимизации эрадикационной терапии инфекции H. pylori могут быть применены для повышения эффективности не только стандартной тройной терапии, но и других режимов антигеликобактерного лечения, а комбинирование этих методов позволяет добиться наилучшего результата у конкретного пациента.
Ключевые слова: Helicobacter pylori, хронический гастрит, эрадикационная терапия инфекции H. pylori.
Для цитирования: Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин А.А., Трухманов А.С., Баранская Е.К., Абдулхаков Р.А., Алексеева О.П., Алексеенко С.А., Дехнич Н.Н., Козлов Р.С., Кляритская И.Л., Корочанская Н.В., Курилович С.А., Осипенко М.Ф., Симаненков В.И., Ткачев А.В., Хлынов И.Б., Цуканов В.В. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых. Рос журн гастроэнтерол гепатол колопроктол 2018; 28(1):55-70
DOI: 10.22416/1382-4376-2018-28-1-55-70
Приложение. Методология разработки клинических рекомендаций
Целевая аудитория данных клинических рекомендаций:
• врачи-терапевты
• врачи общей практики (семейные врачи)
• гастроэнтерологи
• хирурги
• эндоскописты.
Клинические рекомендации отражают мнение экспертов по ключевым вопросам. При изложении рекомендаций использованы следующие уровни достоверности доказательств (табл. 1) и уровни убедительности рекомендаций (табл. 2).
В клинической практике могут возникать ситуации, выходящие за рамки представленных рекомендаций, поэтому окончательное решение относительно тактики ведения конкретного пациента должен принимать лечащий врач, на котором лежит ответственность за лечение.
Таблица 1. Уровни достоверности доказательств (Оксфордский центр доказательной медицины)
Таблица 2. Уровни убедительности рекомендаций (Оксфордский центр доказательной медицины)
Порядок обновления клинических рекомендаций
Рекомендации подлежат регулярному (не реже чем каждые 3 года) пересмотру в соответствии с новыми данными научных исследований в этой области. Состав рабочей группы, участвующей в обновлении рекомендаций, определяет Президиум Российской гастроэнтерологической ассоциация.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
- Какие заболевания вызывает
- Причины
- Симптомы
- Диагностика
- Лечение
- Профилактика
Изображение от ArtPhoto_studio на Freepik
Хеликобактер пилори или Helicobacter pylori в латинском варианте — это бактерия в желудке и 12-перстной кишке, которая была открыта учеными из Австралии Р. Уорреном и Б. Маршаллом, за что они получили в 2005 году Нобелевскую премию.
На сегодняшний день H. pylori считается наиболее распространенной инфекцией хронического типа. В нашей стране инфекцию обнаруживают у 65–92% взрослых1.
Какие заболевания вызывает
Хеликобактер пилори является возбудителем хеликобактериоза — инфекционного заболевания, при котором поражаются слизистые желудка и двенадцатиперстной кишки.
Чтобы адаптироваться и выжить в агрессивной среде желудка, бактерия формирует вокруг себя щелочную среду. Она, в свою очередь, усиливает выделение соляной кислоты железами желудка и снижает секрецию щелочи в 12-перстной кишке. Этот сбой в соотношении кислоты и нейтрализующих её щелочных компонентов приводит к повышению кислотности желудка и началу воспалительных реакций, на фоне чего у многих больных развивается гастрит, у части – язвенная болезнь.
Причины
Несмотря на многочисленные эпидемиологические исследования, точные причины развития болезни ещё до конца не изучены. Предметом спора являются 2 основные точки зрения на этиологию заболевания:
-
Хеликобактер является инфекционным патогенным агентом, т. е. обитает в окружающей среде и становится возбудителем инфекции, заражая человека.
Согласно этой теории, большинство случаев заражения происходит путем передачи инфекции от человека к человеку орально-желудочным или орально-оральным путем. Кроме того, предположительно, возможно заражение через воду, пищу, домашних животных и насекомых.2 -
Бактерия относится к условно-патогенной флоре, т. е. к естественным обитателям здорового организма, которые могут вызвать заболевание только при наличии дополнительных факторов: резком увеличении численности бактерий или при снижении иммунитета.
Симптомы
Присутствие бактерии H. pylori может быть бессимптомным носительством. Жалобы возникают, когда развиваются воспалительных процессы на слизитой желудка. Гастрит и язва, ассоциированные с хеликобактериями, ничем не отличаются от обычных, возникших без участия этой бактерии.
Проявления гастрита:
-
тошнота;
-
отрыжка;
-
дискомфорт в животе (тяжесть, изжога, вздутие);
-
боли в эпигастральной области;
-
учащение стула (не всегда);
-
рвота (редко);
-
повышение температуры тела (очень редко).
Пациент может долго быть носителем Helicobacter pylori, однако иногда первые проявления обнаруживаются уже через 1,5–2 недели после проникновения возбудителя. Зачастую симптоматика появляется у пациентов с функциональной диспепсией (т. н. диагнозом исключения) — заболеванием, вызывающим дискомфорт в желудке без видимых на то причин.
Для язвы характерны вышеперечисленные симптомы, но боли бывают интенсивные, выраженные, усиливающиеся натощак и после приема грубой пищи.
Диагностика
Выявлением, лечением и профилактикой заболевания занимается гастроэнтеролог. Врач собирает симптомы, проводит осмотр, назначает обследования, выставляет диагноз и составляет схему лечения.
Для подтверждения наличия Хеликобактер пилори используются следующие методы:
-
Серологический анализ крови на выявление антител (иммуноглобулинов класса G) к H. pylori. Как к любому микроорганизму, вырабатывается иммунный ответ в виде образования специальных клеток – антител, нацеленных на уничтожение именно хеликобактерий. Иммуноферментный анализ (ИФА) показывает есть или нет в крови такие антитела, наличие указывает на то, что организм встречался с возбудителем ранее.
-
Серологический анализ кала на определение антигена к Helicobacter pylori. Чувствительность приближается к 92%.
-
Дыхательный уреазный тест. Пациент выпивает раствор мочевины, затем в выдыхаемом воздухе измеряется уровень меченых изотопов углерода. Исследование базируется на ферментативной активности Хеликобактер пилори. Дыхательный уреазный тест проводится как с целью диагностики заболевания, так и для определения эффективности лечения. Чувствительность достигает 96%, является лучшим методом для первичной диагностики.
-
Эзофагогастродуоденоскопия с биопсией. Пациент проглатывает гибкий зонд, оснащенный источником света, камерой и инструментами. На экран выводится четкое и крупное изображение состояния слизистой оболочки пищевода, желудка и 12-перстной кишки. При наличии признаков гастрита (воспаления) – покраснения и отека – проводится биопсия. Для язвы характерно определение язвенного дефекта – углубления с приподнятыми краями, на дне могут быть кровоизлияния или белесые нити фибрина. Врач отщипывает микропрепараты тканей из разных точек желудка для подтверждения наличия микроорганизмов в эпителии.
Цитологическое изучение биоптатов. Микроскопические кусочки эпителия, полученные при биопсии, фиксируют на стеклах и с помощью микроскопа изучают состав клеток на предмет обнаружения возбудителя и признаков воспаления. Чувствительность доходит до 95%.
Уреазный тест на биоптатах. Для выявления Хеликобактер пилори в тканях желудка используются индикаторы – окрашивание в желтый цвет указывает на положительный результат, что является основанием для назначения лечения. Чувствительность составляет от 61 до 92%, отрицательный результат не дает гарантии, что Helicobacter pylori отсутствует в организме.
К дополнительным анализам, назначаемым при клинике гастрита и язвы, относится общий анализ крови, в котором будут обнаруживаться повышение лейкоцитов и СОЭ, возможно снижение гемоглобина и эритроцитов.
Лечение
Ранее не было единого мнения о необходимости проведения антихеликобактерной терапии, затем была накоплена большая научная база о негативном влиянии Helicobacter pylori на слизистую оболочку.
Что дает устранение Хеликобактер пилори:
-
излечение гастрита в острой или хронической форме;
-
предупреждение предраковых изменений – атрофии, метаплазии;
-
предотвращение 90% случае рака желудка некардиального отдела.
Лечение Хеликобактер пилори проводится обязательно комплексно, согласно утвержденным схемам лечения. Схемы включает такие препараты, как:
-
Антибиотики. Непосредственно уничтожают возбудителя.
-
Ингибитор протонной помпы (ИПП). Важный компонент, уменьшающий выделение желудочного сока. За счет этого улучшается заживление слизистой оболочки, повышается активность антибиотиков и снижается сопротивляемость H. pylori. Одним из самых часто назначаемых средств является омепразол – эффективный, доступный препарат.
-
Висмутсодержащие средства. Образуют пленку на слизистой, защищая воспаленный участок от агрессивного содержимого желудка.
-
Препараты, нормализующие микрофлору. Пробиотики включают в состав эрадикационной терапии (схема лечения для полного уничтожения Helicobacter pylori) для повышения её эффективности и профилактики побочных эффектов со стороны ЖКТ.3
Помимо медикаментозной терапии, важнейшую роль во время лечения заболеваний, вызванных H. Pylori, играет питание. 90% успеха в выздоровлении – это строжайшая диета. Например, лечебный стол №1 по системе М.Певзнера. Он показан при язвенной болезни желудка и двенадцатиперстной кишки, остром и хроническом гастрите. Диета назначается на 2–3 месяца с дробным режимом питания 4–5 раз в день небольшими порциями. Меню содержит преимущественно теплую пищу в полужидком или желеобразном виде, ограничено потребление поваренной соли. Рекомендованы супы из протертых овощей и круп, каши, пюре, омлеты и др. Исключены жареные и острые блюда, копчености, соленья и консервы, бобовые, черный хлеб и сдоба, газированные напитки и алкоголь.
Профилактика
Полностью защититься от Helicobacter pylori вряд ли получится – обсеменение ею близится к 100%, микроорганизм постоянно передается от человека к человеку. Что можно предпринять для того, что снизить риск заражения и уменьшить возможные негативные последствия:
-
соблюдать правила личной гигиены;
-
питаться по возможности максимально полезной едой;
-
своевременно проходить медицинские осмотры;
-
лечить болезни желудка и кишечника своевременно и полностью;
-
укреплять иммунитет.
Хеликобактер пилори погибает при кипячении и в дезинфицирующих растворах, поэтому обработка предметов (в случае необходимости) также поможет с точки зрения профилактики.
Литература:
-
Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин А.А., Трухманов А.С., Абдулхаков Р.А., Алексеенко С.А., Дехнич Н.Н., Козлов Р.С., Кляритская И.Л., Курилович С.А., Осипенко М.Ф., Симаненков В.И., Хлынов И.Б. Лечение инфекции Helicobacter pylori: мейнстрим и новации (Обзор литературы и резолюция Экспертного совета Российской гастроэнтерологической ассоциации 19 мая 2017 г.). Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2017;27(4):4-21
-
World Gastroenterology Organisation. World Gastroenterology Organisation Global Guideline: Helicobacter pylori. Peter Katelaris , Richard Hunt, Franco Bazzoli, Henry Cohen, Kwong Ming Fock, Manik Gemilyan, Peter Malfertheiner, Francis Mégraud, Alejandro Piscoya, Duc Quach, Nimish Vakil, Louis G. Vaz Coelho, Anton LeMair. 2021 May
-
Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин А.А., Трухманов А.С., Баранская Е.К., Абдулхаков Р.А., Алексеева О.П., Алексеенко С.А., Дехнич Н.Н., Козлов Р.С., Кляритская И.Л., Корочанская Н.В., Курилович С.А., Осипенко М.Ф., Симаненков В.И., Ткачев А.В., Хлынов И.Б., Цуканов В.В. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2018;28(1):55-70.






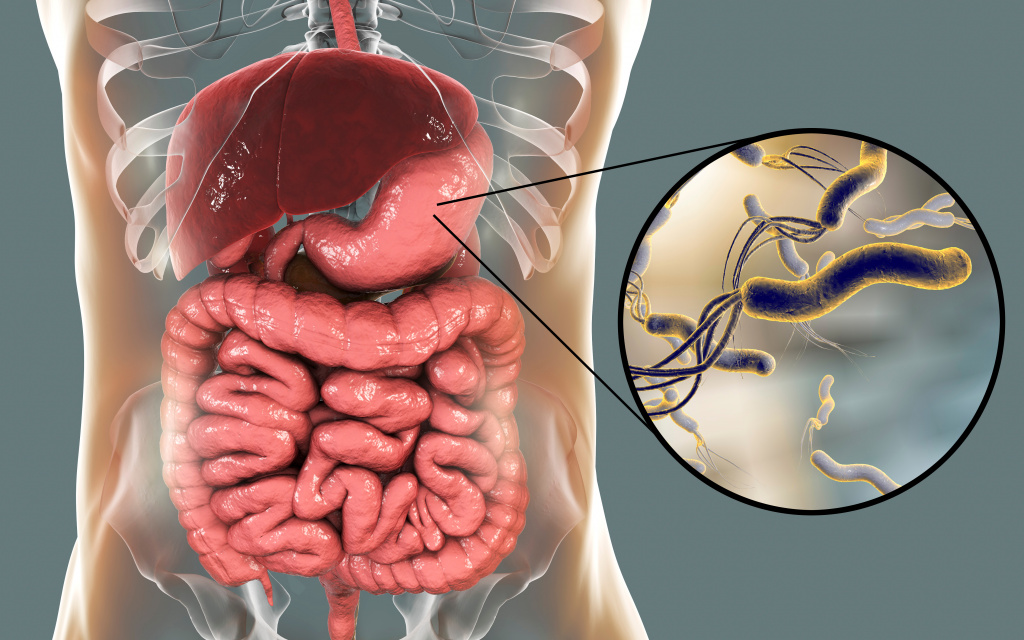

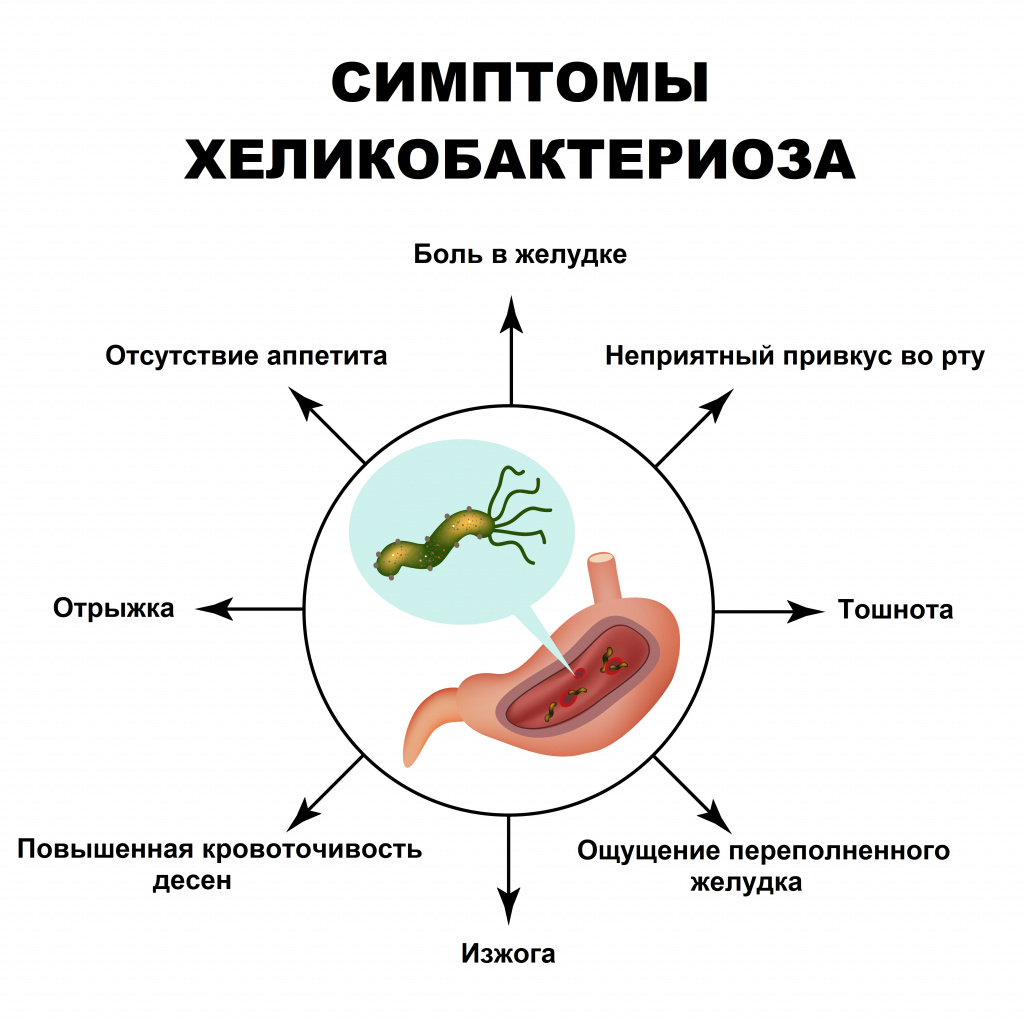







 http://www.iarc.fr/en/publications/
http://www.iarc.fr/en/publications/